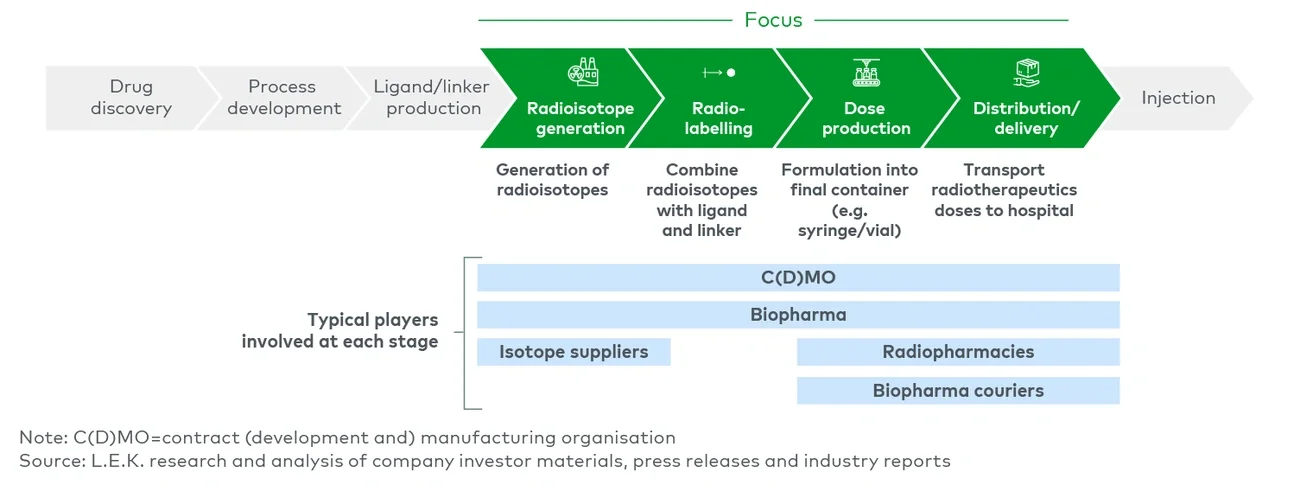
放射性标记:CDMO服务的核心环节
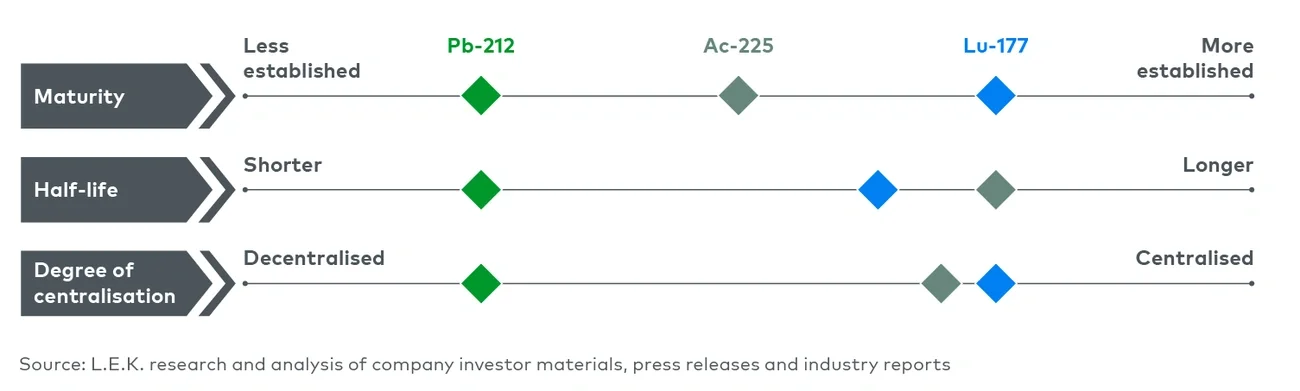
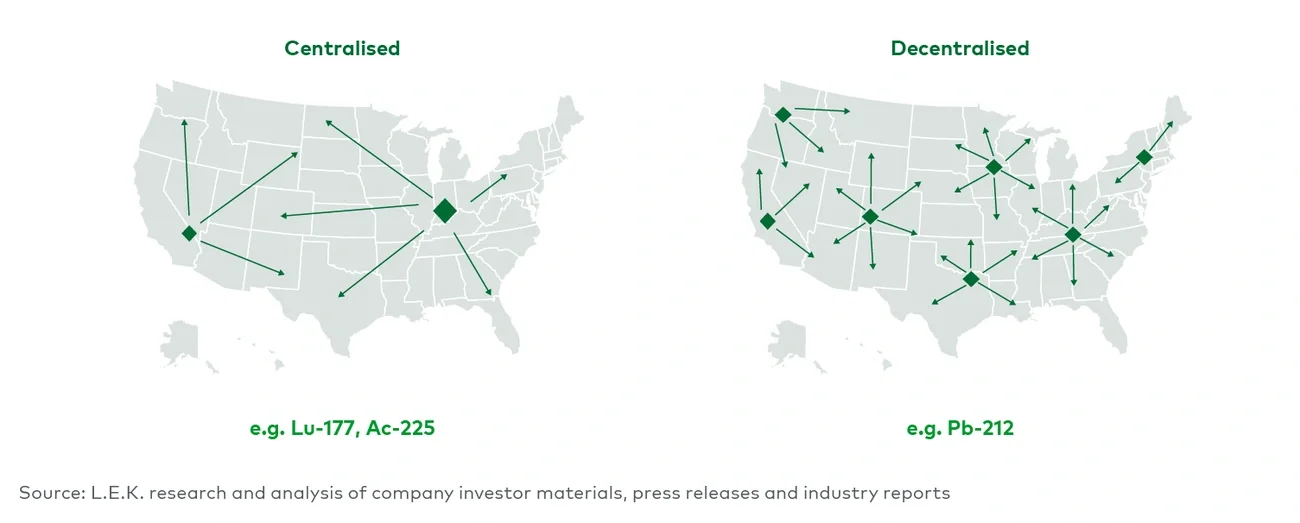
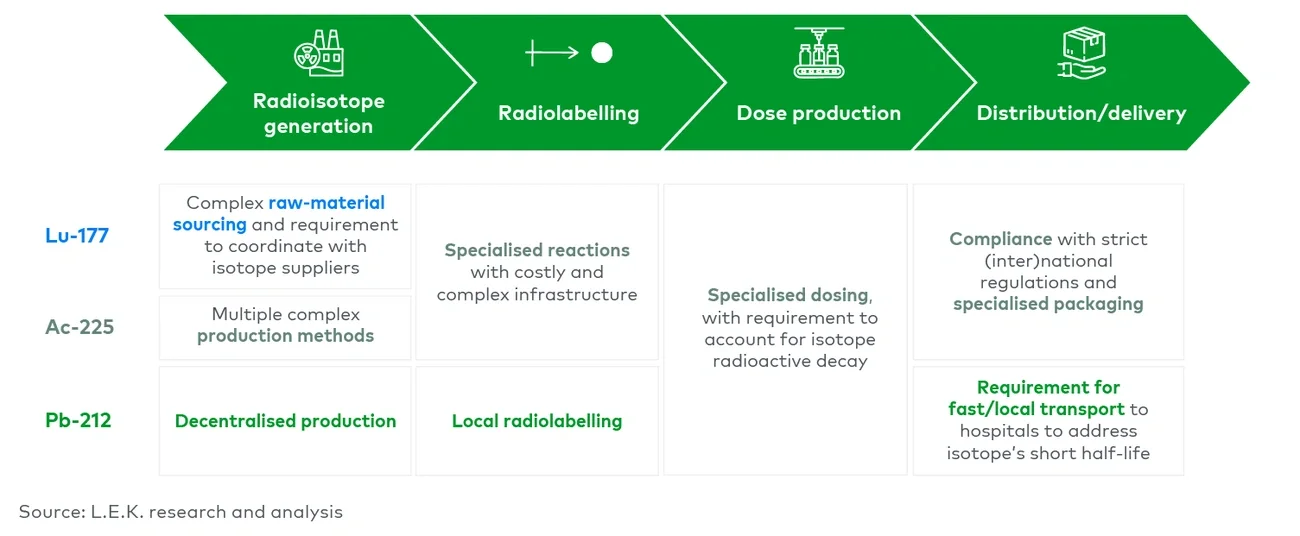
放射性标记是将放射性同位素通过螯合剂与靶向配体连接的过程。在Lu-177和Ac-225的应用中,由于它们半衰期较长,这一工艺通常可以在集中化设施中进行。具体的标记条件取决于所用的同位素和螯合剂组合,但通常要求高温高压,同时还需严格遵守放射性化合物操作的安全规范。
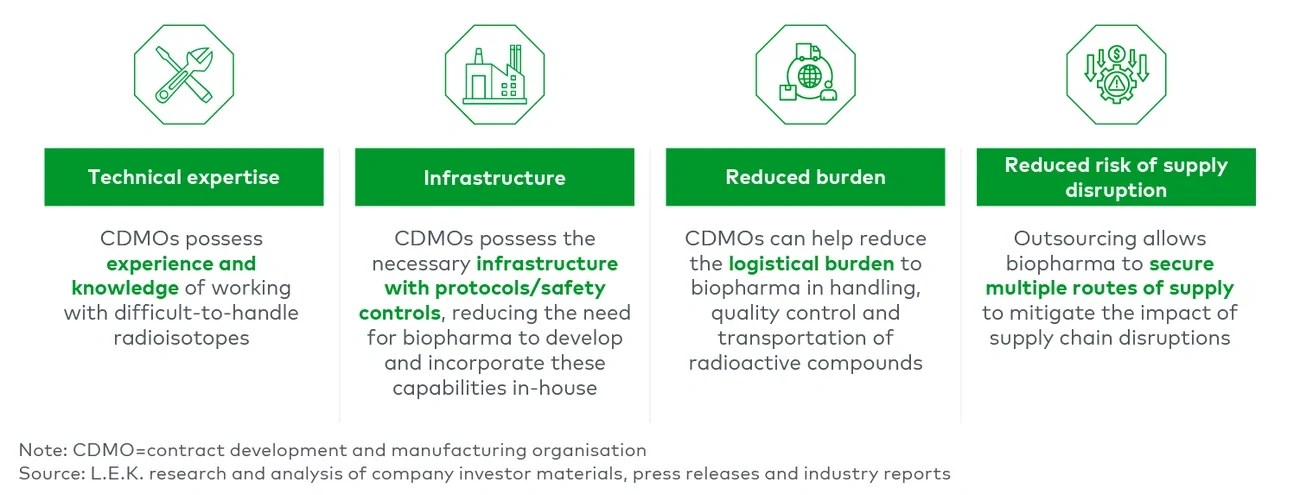
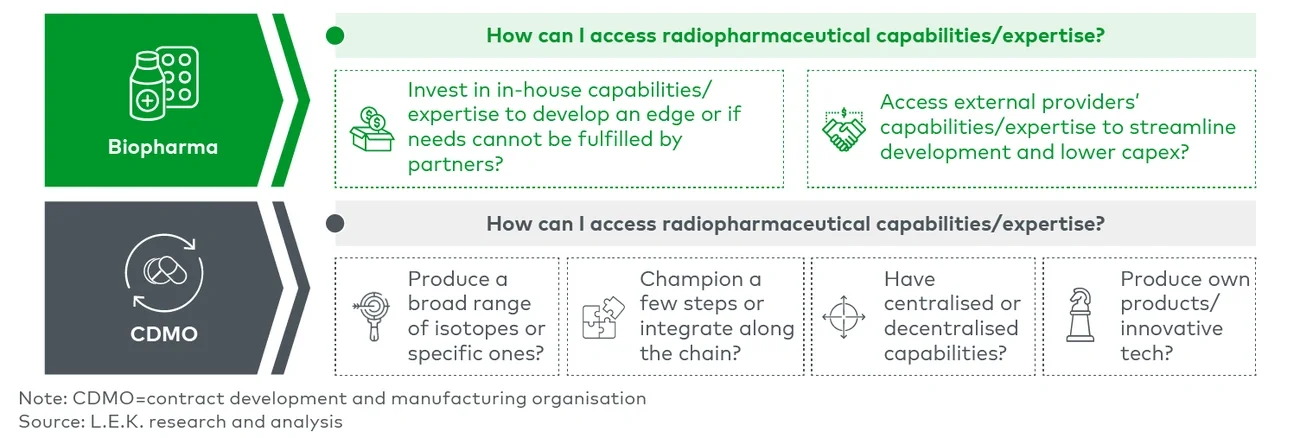
尽管一些生物制药公司可能会出于供应安全和质量控制的考虑,倾向于在内部进行放射性标记,但CDMO在这一过程中依然能发挥关键作用,帮助企业避免高昂的投资成本以及基础设施建设的复杂性(例如屏蔽实验室、热室、手套箱等操作系统),同时简化相关操作流程。CDMO还具备在螯合技术以及将靶向化合物与放射性同位素最终连接方面的深厚专业知识,这些能力对于新进入者而言往往难以在短时间内建立。目前活跃于该领域的一些CDMO代表包括SpectronRx和NorthStar。中国核药CDMO领域正步入快速发展阶段:传统核药企业东诚药业通过并购米度生物,布局一站式核药CRDMO平台;药明康德、昭衍新药等综合性CRO和CDMO龙头也加快进入核药领域,拓展业务边界;与此同时,国通新药等一批专注于核药CDMO的新兴企业不断涌现,推动产业链专业化发展。
由于Pb-212的半衰期较短,因此必须在本地进行放射性标记,从而对地理覆盖范围提出了更广泛的要求。CDMO在满足这种本地化放射性标记需求方面可以发挥关键作用,正是由于该同位素的时间敏感性所致。
从更广义的角度来看,放射性衰变的特性决定了放射性药物CDMO需要全年更频繁地进行小批量生产,这与其他治疗类型通常可以进行大批量、低频率生产的模式形成对比。这种更为持续的生产节奏带来了更高的设施使用率,也可能使得放射性药物CDMO在运营模式和盈利水平上,与传统治疗方式的CDMO存在明显差异。
扩展CDMO能力至剂型制备与物流配送
在完成放射性标记之后,化合物需被制备成可直接注射的注射器或小瓶剂型。这一阶段技术要求较高,因为必须精确计量治疗剂量,以在最大程度提高疗效的同时,降低毒性风险。由于放射性同位素会持续衰变,剂量的制备过程必须考虑这种衰减,以确保患者接受到预期的放射剂量。
对于不具备内部能力的企业,CDMO可以全程负责这一过程。此外,一些放射性药房也能承担这一步骤,有些设施甚至同时具备CDMO与放射性药房的双重职能。
配送与交付是患者接受治疗前的最后一个环节。鉴于同位素的放射性衰变特性,这一过程必须被精细管理。运输不仅要遵守严格的国家和国际法规,还需使用专用包装材料以确保运输过程中的安全性。根据具体的同位素类型以及价值链中各方的能力,最终剂量送达治疗现场之前,可能会经历多方的中转,包括放射性中间体或成品的转交。
放射性同位素的半衰期是物流规划中最关键的参数之一,这也凸显了一体化服务提供商的重要性。以Orano Med为例,其为Pb-212开发了专门的物流系统。该公司在北美设立的ATLab大规模生产设施就选址于印第安纳州,靠近主要的国内外配送枢纽和快递公司(如FedEx),以实现快速运输至医院,从而应对Pb-212仅有10.6小时的半衰期。在拓展中国核药市场的过程中,跨国企业亟需与本土放射性药物供应链伙伴展开深度协作。例如,诺华已与上药和重药达成战略合作,联合打造覆盖全国的药品供应与临床应用支持体系,促进其重磅Lu-177产品在中国的商业化落地。
这一环节的挑战也为生物制药行业带来了新机遇,例如可能促使更多生物制药专属快递服务商扩展其业务至放射性治疗药物领域,利用其在物流速度与优化方面的优势。在欧美市场,像Life Couriers这样的公司目前已提供放射性药物的物流服务,并可能将业务拓展至其他高敏感度的生物产,如活细胞运输,等相关领域。最终,在放射性同位素被运送至医院和治疗中心之后,这些机构在最后的处理、储存与患者给药方面也扮演着至关重要的角色。