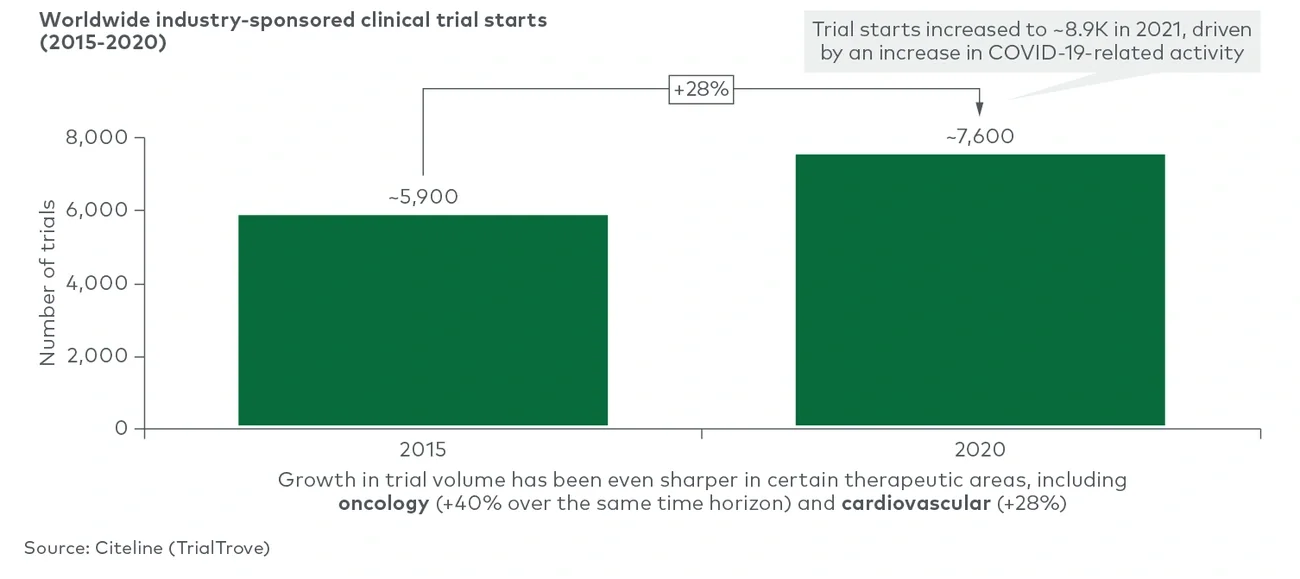
得益于技术的进步、新药物模式的出现以及有利于行业扩张的融资环境,生物制药行业在过去十年中实现了大幅增长。在此背景下,临床试验管线不断增多,行业生态不断完善,进一步刺激了增长。肿瘤等竞争激烈的治疗领域的全球增长尤为显著,每个资产都需进行不同数量和范围的临床试验,临床试验市场格局因此变得愈发复杂。中国的情况亦是如此,2021年肿瘤领域的临床试验数量占比高达40%,其中包括各种常见和创新的药物靶点。随着临床试验管线数量和活跃度的增加,市场迎来前所未有的激烈竞争。但众所周知,面对越来越密集的药物开发格局,相关方(临床试验申办方、试验地点和患者)正面临一系列挫折和挑战。
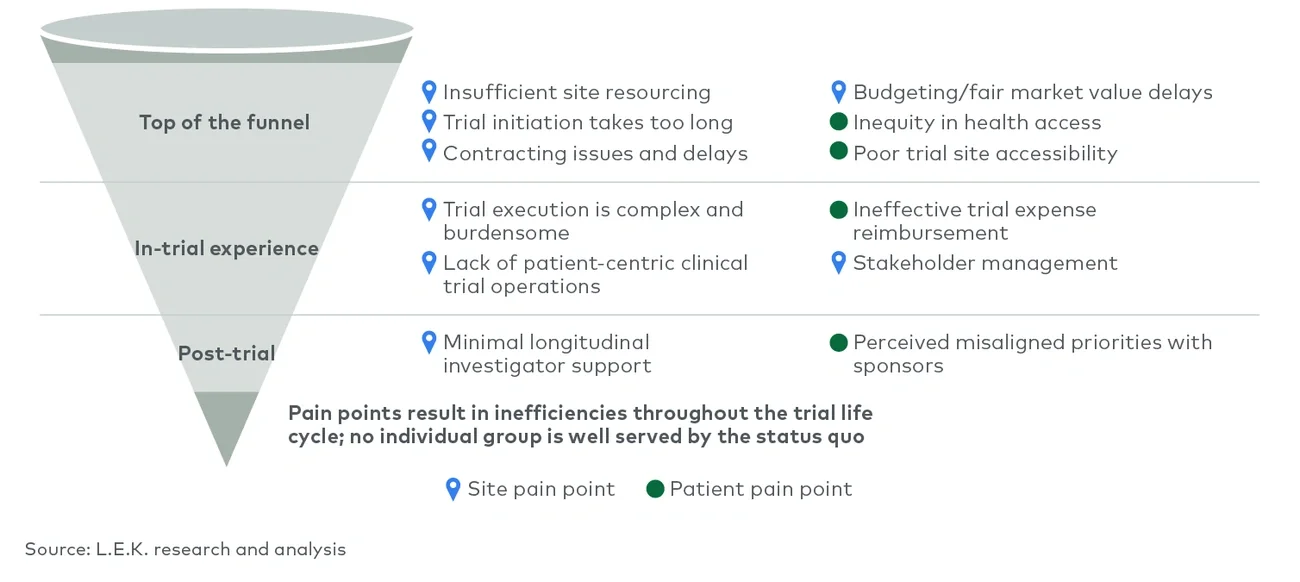
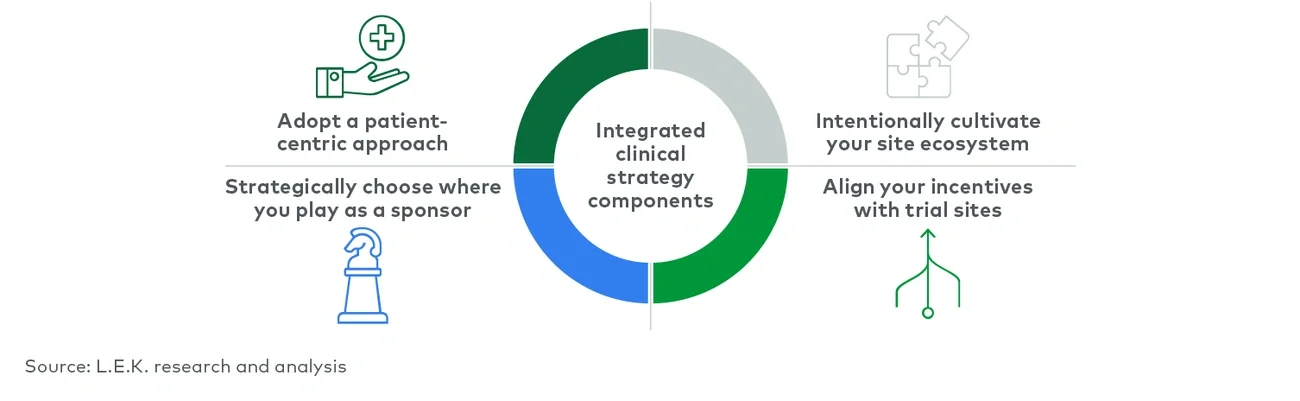
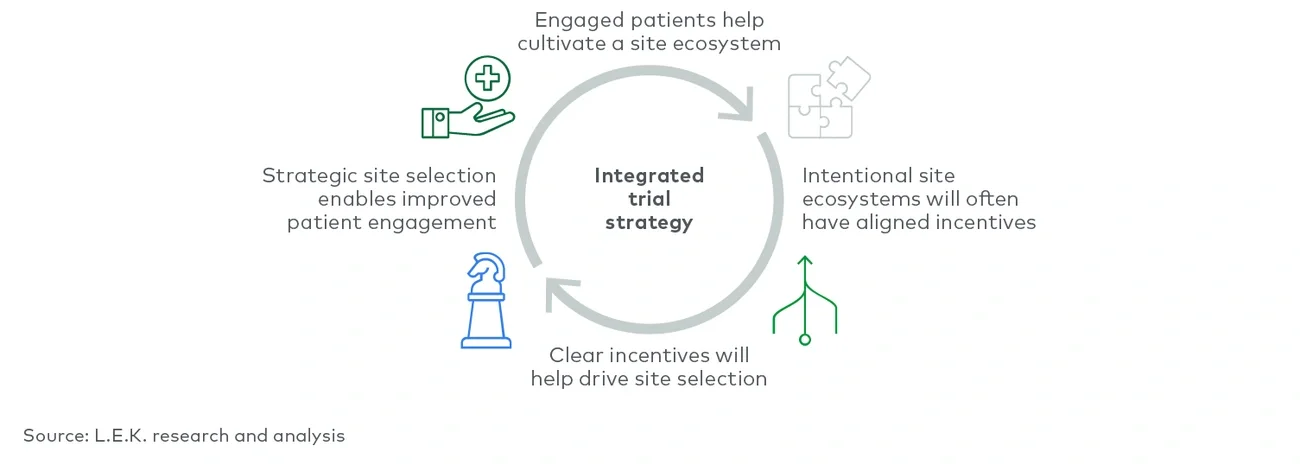
当前的临床试验模式主要集中在让足够多的患者接受试验性疗法,从而达到研究终点。但这种模式并不能提供一种协调且全面的方法,让临床试验满足所有相关方的需求,也未能满足患者、试验点和主要研究人员的不同需求。全面制定一种协调整合的临床试验方法,能够让临床试验申办方更好地制定相关解决方案并使其差异化,以更好地维系与各相关方的关系。