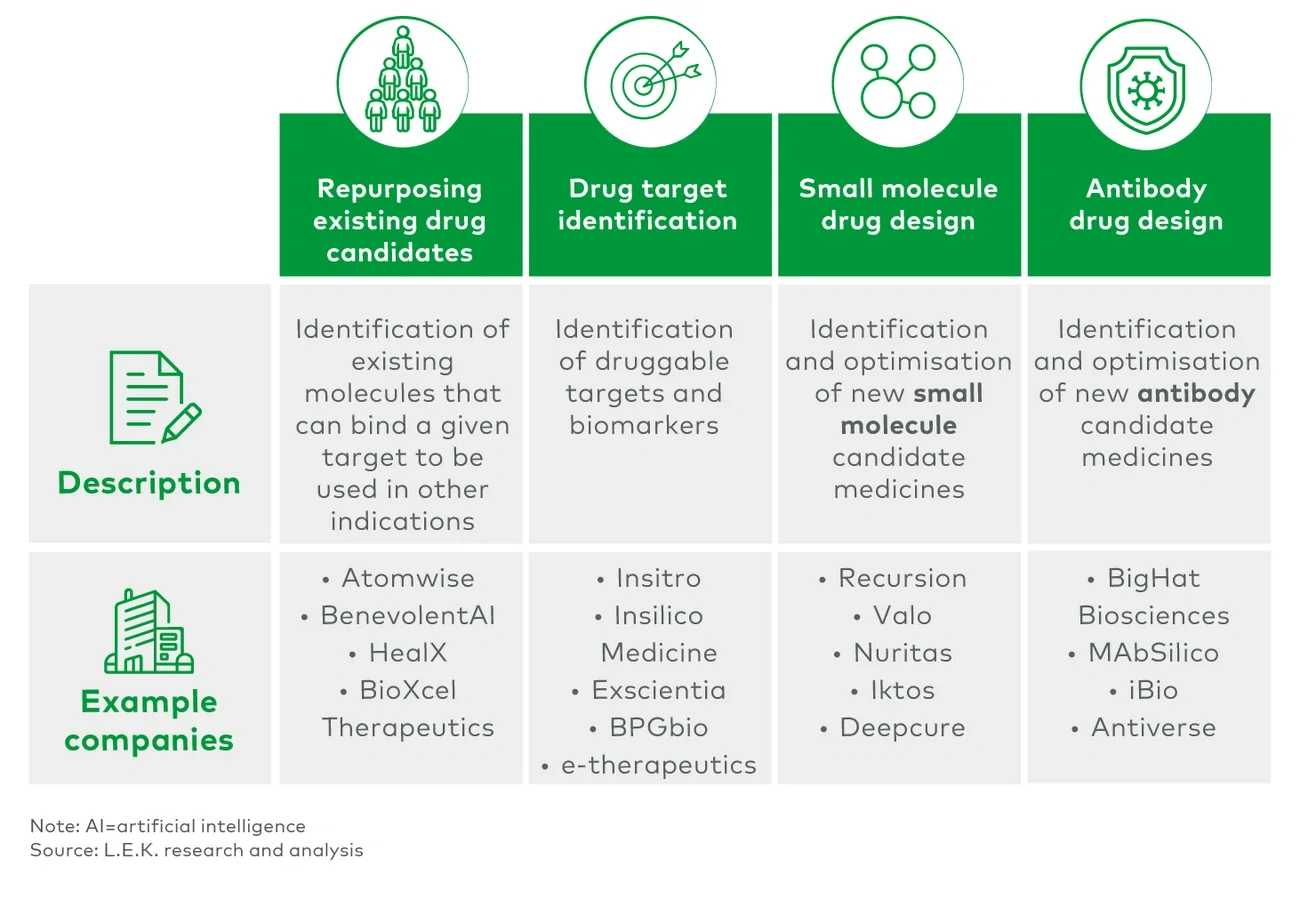
1. ドラッグ・リポジショニング
これまでのところ、創薬の観点からAIの力が最も発揮されるのはおそらく、ドラッグ・リポジショニングの場面である。つまりAIを使うことで、既存の分子に対する別の適応症を迅速に同定できるのである。現在、250社を超える企業がAIを使ってドラッグ・リポジショニングに取り組んでいる。COVID-19により、この迅速かつ柔軟なアプローチを創薬に適用するという、またとない機会が得られることになった。
バリシチニブは関節リウマチを適応症としたヤヌスキナーゼ阻害薬であるが、BenevolentAIでは、同社のナレッジグラフプラットフォームを用いてCOVID-19に対する治療薬候補としてこれを同定した。2020年、入院患者を対象としたCOVID-19治療薬として、米国食品医薬品局(FDA)によりバリシチニブの緊急使用許可が認められた。その後、4つの無作為化臨床試験の結果に基づき、2022年には全面的に承認されることとなった。
AIによるドラッグ・リポジショニングで特定された化合物の多くは、現在も臨床試験で評価が行われている。データが多様化しアクセス性の向上に伴い、データの可用性と品質は今後改善すると予想されており、この分野の取り組みはさらに活発化する見込みである。
2. 創薬標的の同定
AI技術により、分子疾患モデルを迅速に構築できるとともに、従来の方法よりも効率的に新薬の開発につながるような標的やバイオマーカーを同定できるようになった。複数の非構造化データセットの統合は困難であるものの、膨大な量の生物医学データが利用可能となっている。AIを使用すれば、学術論文やオミクスデータベースに加え、画像や実臨床下の患者データなど、非構造化データセットから所見を抽出・分析することができる。ナレッジグラフを使えば、分子間にある新たな関係が確認できる。ただし、基礎となるデータセットの標準化やラベリングの質によって、これらのアプローチの能力には限界がある。
創薬標的の同定という点でAIを使用した初期のプログラムでは、発見と前臨床開発のステージを経て、新たな疾患-標的の関連性をAIが同定した20種類以上の薬が、第I相、第II相試験へと進んでいる。企業がデータセットを拡大し、その結果をAIアルゴリズムにフィードバックしていくにつれ、新たな疾患-標的の関連性を有する、あるいはまったく新しい標的を有する薬が登場する数も増えていくと予想される。
3. 低分子薬の設計
利用可能な化学構造データを使用することで、AIは複雑な化学特性をシミュレートしたり、従来の方法よりもはるかに迅速かつ正確に、薬物の構造を設計したりできる。このユースケースの場合、企業はAIを使用して既存のケミカルライブラリをスクリーニングしたり、新規の化学物質を設計したりできる。このユースケースでは、基礎となるデータセットの可用性と使いやすさが引き続き大きな課題となっている。数十億の化合物からなる化学空間全体と比べれば、トレーニングセットは比較的小規模であるからだ。
加えて、標的クラスが違えばデータ可用性にも差が出てくる。つまり、キナーゼとGタンパク質共役受容体は最もよく研究されているが、これにより汎用性の高いモデルの開発や結果として得られる創薬候補の新規性に限界が生じるのである。
低分子の場合、個々のAI駆動型ツールが既に医薬品設計プロセスに不可欠な要素となっており、より大規模な予測ソリューションの開発が反復的に行われている。現時点では、AIを用いて設計された抗体よりもAIを用いて設計された低分子の方がはるかに多い。ExscientiaやInsilico Medicineといった企業による臨床プログラムは、AIの設計に基づく低分子薬の第1波の例であり、現在第II相試験が実施されている。その結果が、このユースケースの成熟度と将来性を最初に物語ることになる可能性が高い。
4. 抗体医薬品の設計
既存の構造の最適化と新規の候補薬の設計のいずれの場合でも、AIを用いたユースケースとして抗体設計の数は増加している。現在までに、臨床使用にまで至ったAIの設計に基づく抗体医薬品は殆どない。低分子薬の設計と比較してこれらの分子はより複雑であるため、独自の課題が存在する。例えば、より大規模なモデルを実行するのに必要となる計算能力などである。抗体設計のAIモデルには、抗体配列や抗体-抗原ペアのデータセットの可用性による限界もある。さらに、トレーニングデータの大部分が従来の抗体設計アプローチで使用したものと同一のライブラリに由来しているため、特異性と親和性のバランス調整など、従来からある課題の多くがそのまま残されている。
抗体医薬品の設計を目的としたAIに注力する研究者や企業からなるエコシステムは成長している。過去1年の間にも、大手製薬企業が社内ケイパビリティの強化や、スタートアップ・大手テック企業との提携を立て続けに発表している。
最近では、Xaira Therapeuticsが10億米ドルを超える資金を調達した。その計画では、タンパク質や抗体の設計を目的とした有力な拡散モデルの設計経験がある研究者を、ゲノミクスおよびプロテオミクスグループとともに採用し、de novo抗体に焦点を当てた開発に取り組むことになっている。AIプラットフォームと製薬企業との継続的な連携に加え、標準化されたオープンソースデータの増加により、このユースケースの成熟度が高まることが予想される。
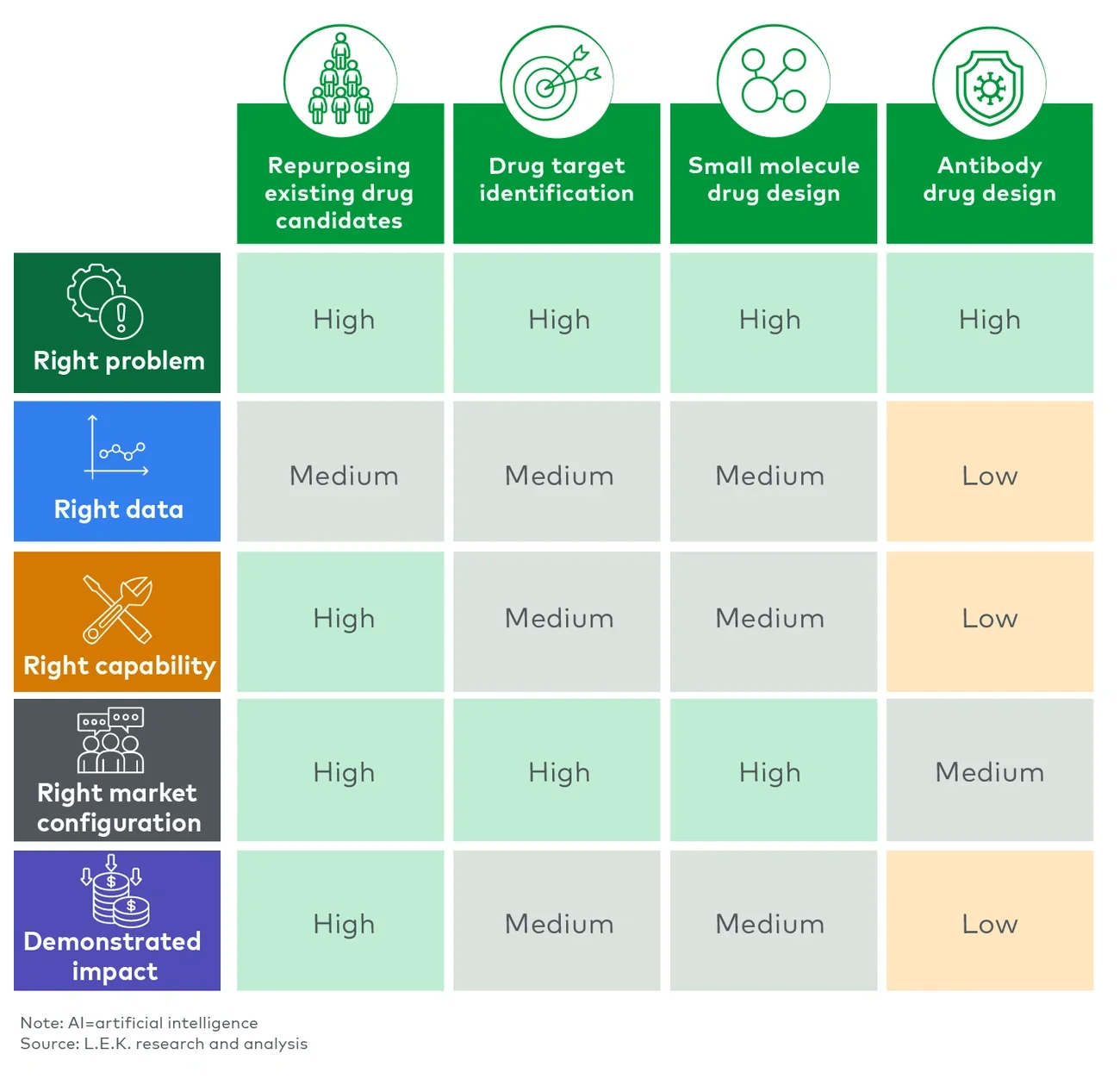
見通し:ユースケース全体におけるAIの成熟度
ライフサイエンス分野におけるAIの成熟度の見通しはそれぞれ異なり、ユースケースによってばらつきがある(図4を参照)。ドラッグ・リポジショニングや創薬標的の同定といったアプリケーションでは大幅な進歩がみられるものの、抗体医薬品の設計などでは依然として比較的初期段階にあると考えられる。