4. 診断薬(Dx)の発売戦略を別途構築します
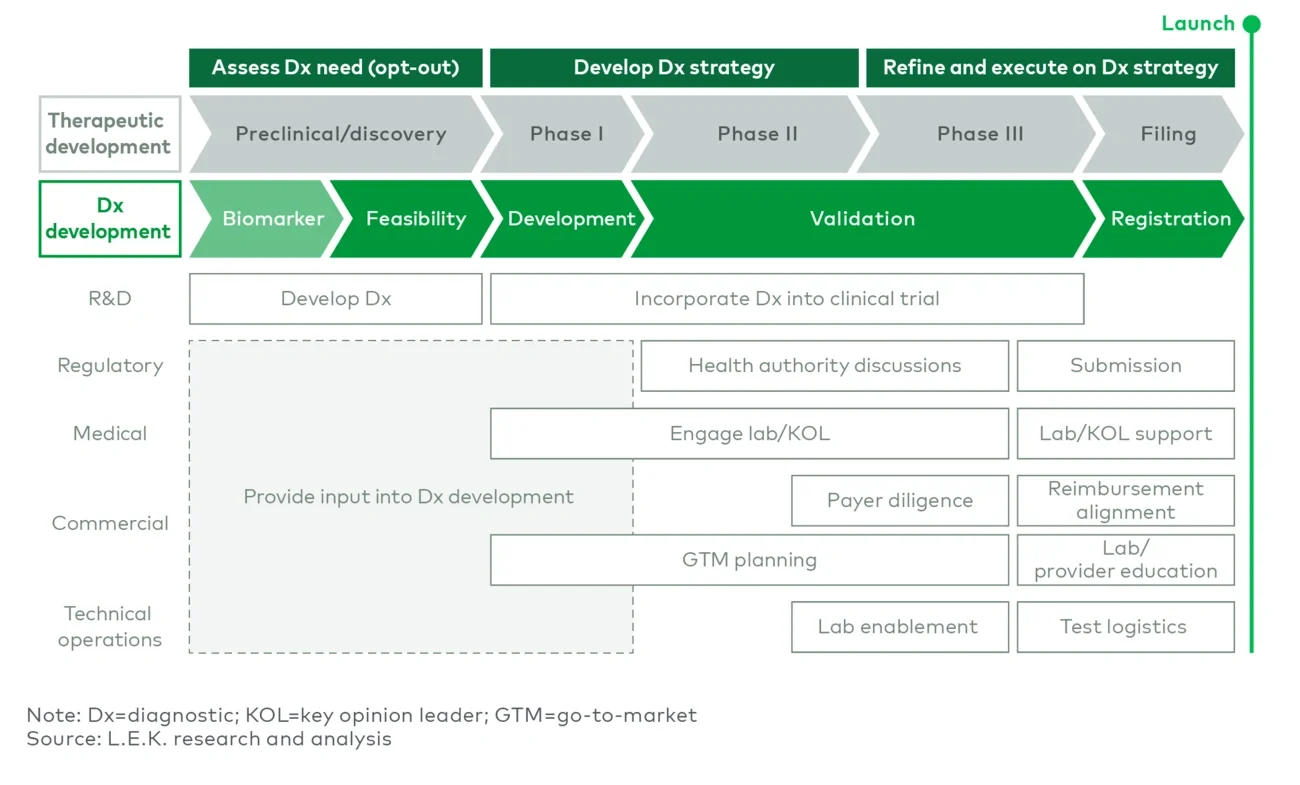
精密医療リーダー企業は、診断薬のローンチと治療薬のローンチを相互に関連しつつも、別個のプロセスと明確に区別して実行しています。両者は異なるステークホルダー層と課題を抱えており、それぞれに特化したアプローチが求められます。主要なCDxのステークホルダーは多岐にわたり、治療薬のステークホルダーとは大きく異なります。例えば、病理医と処方を担う腫瘍内科医を比較すれば、その違いは明らかです。したがって、認知度向上や処方意欲の促進には、明確にターゲットを絞ったアウトリーチ活動が最も効果的です。
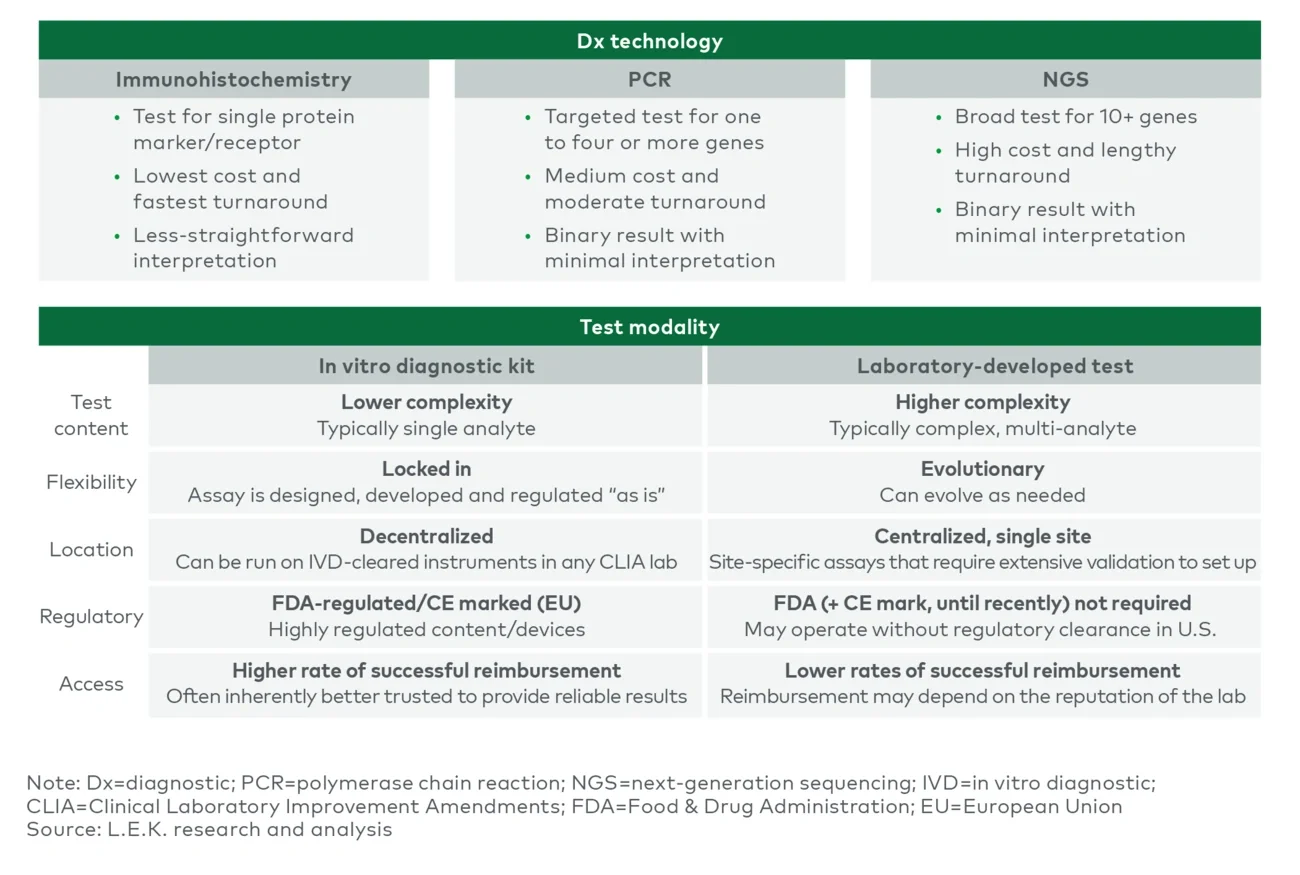
特に新規CDxのように検査が複雑な場合、ローンチ戦略では、必要な機器や関連技術への対応、LDTのサポート体制、検体前処理に関するガイダンスなど、検査室における実務上の要件を慎重に考慮する必要があります。また、市場アクセス戦略も早期に統合し、償還や流通経路に関する課題に先手を打つことが重要です。
理想的には、企業は発売計画を策定する際に、診断薬と治療薬の発売戦略の相互作用をあらかじめ考慮すべきです。例えば、治療薬において一般的な「治療を受ける患者数」に基づく販売インセンティブは、精密医療環境では適切ではない場合があります。この分野では、スクリーニングを受ける患者数のほう
がより重要な成果指標となることが多いからです。このように、診断薬に特化した発売戦略を独自に構築することで、より広範な採用を促進し、精密医療における総合的な成功機会を高めることが可能となります。
5. パートナーの能力を戦略的に活用しつつ、社内の専門性を育成する
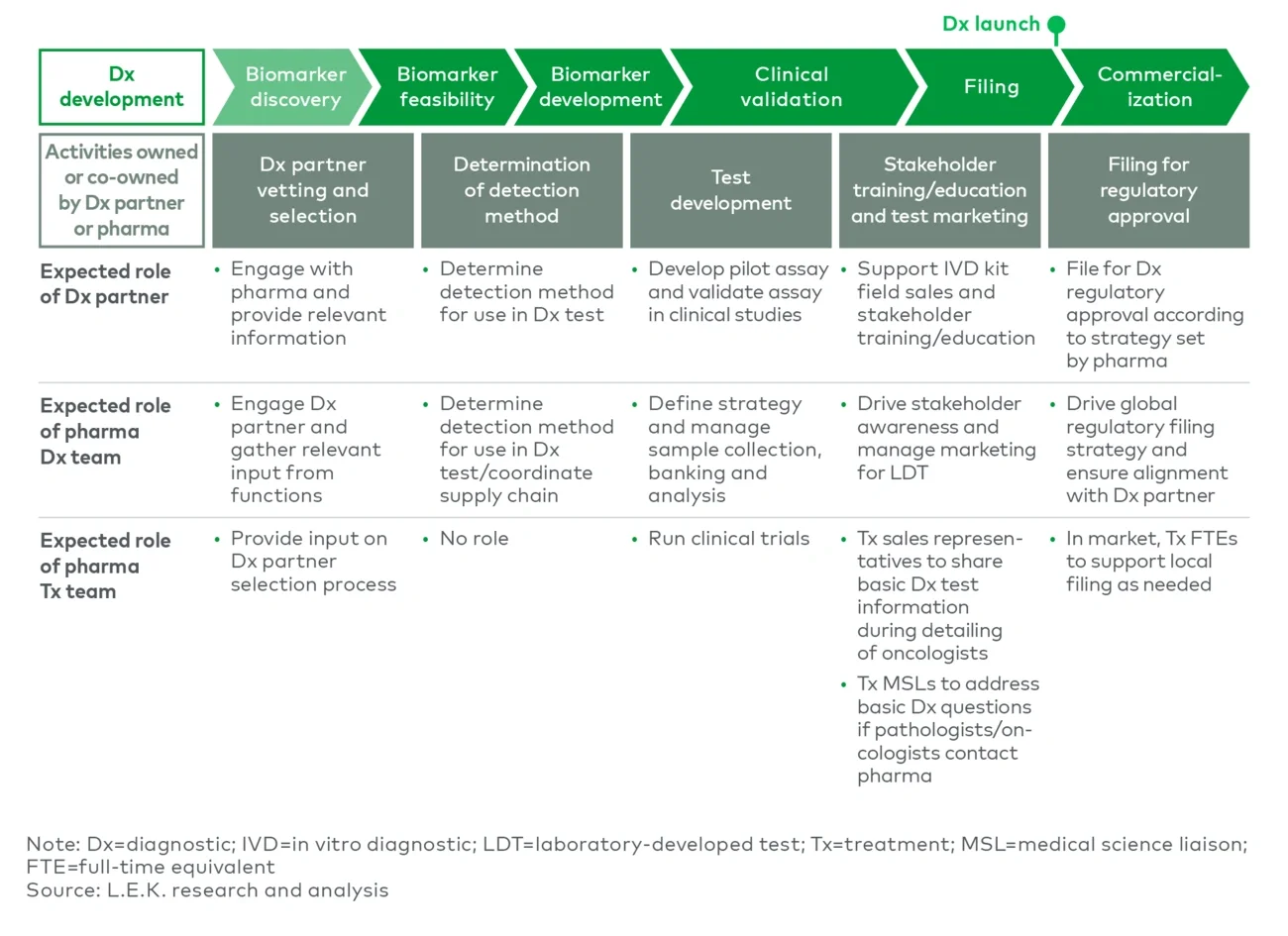
製薬企業は、診断薬の開発、申請、製造に関する専門知識を有する重要なパートナーの能力を意図的 かつ計画的に活用しながら、十分な監督体制を整えることが重要です。組織の規模や既存の能力によっては、バイオマーカーの選定、検査開発、データ解析、診断薬の販売などの領域で社内のリソースが不足する場合があります。一方、治療薬チームとの密接な連携が必要な活動(例:サンプル収集や保管)や、戦略的性質を持つ活動(例:市場アクセスや価格戦略)は、社内で直接管理する方が望ましい場合もあります。
パートナーと連携する場合であっても、バリューチェーン全体を通して診断薬特有の専門知識を持つ専任の社内リソースを確保することが不可欠です。診断薬と精密医療用治療薬の両方を深く理解する専門家は希少であり、需要が高いため、早期からの人材確保と育成計画が極めて重要になります。外部パートナーの専門知識と社内の基盤知識の適切なバランスを見極めることも成功の鍵です。パートナー企業 は、製薬企業の戦略的文脈を十分に理解せず、検査最適化や上市後の活動に十分な投資を行うインセンティブを欠く場合もあります。そのため、内部の監督機能を強化し、パートナー企業と緊密な連携を維持することが不可欠です(図7参照)。