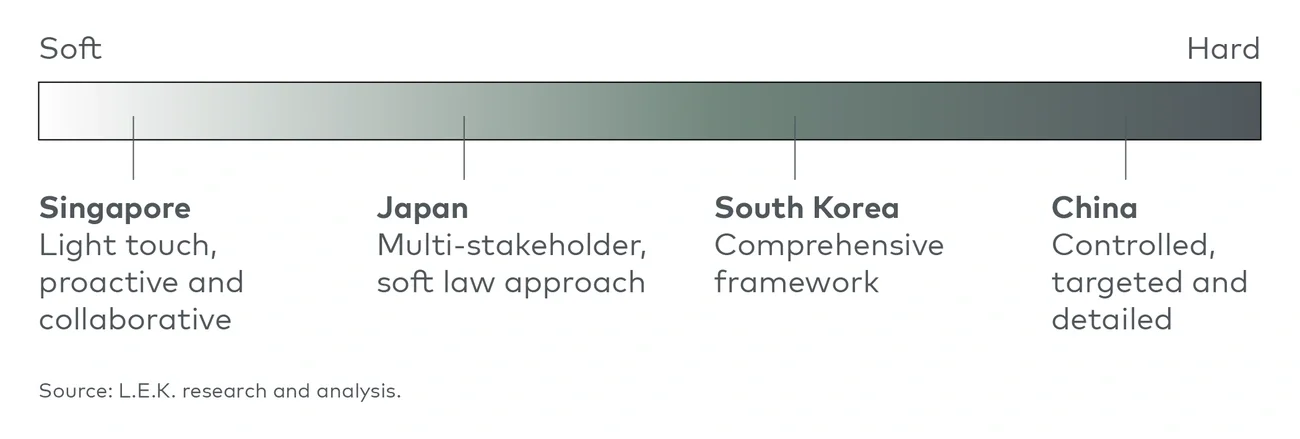
新加坡:宽松、务实、循序渐进
生成式人工智能工具的发展和应用有望帮助新加坡医疗行业解决一系列燃眉之急。政府预测显示,新加坡到2030年需要增加40%的医务工作者,以服务老龄化人口。生成式人工智能工具能够帮助缓解迅速激增的医务人员需求。1
新加坡对生成式人工智能的发展采取了积极主动的监管方式。新加坡政府于六月份发布了一份讨论文件,提出监管政策要聚焦于技术工具的发展、相关标准的制定以及整体技术方向。新加坡在生成式人工智能的监管上一向采取协作的方式,强调让行业参与者自愿接受监管。
该方式的核心是开发了一套名为“AI Verify”的治理测试框架,这一框架借鉴了国际标准和准则,旨在让行业参与者能够自愿评估和验证其人工智能系统。2通过让科技行业巨头公司参与其中,新加坡政府旨在利用整个科技行业的专业知识和经验,来制定健全的人工智能标准和实践准则,以引导人工智能工具的负责任使用。新加坡卫生部的专用IT系统(2023年7月更名为 Synapxe)就是一个很好的例子,通过与国家电子健康记录系统(National Electronic Health Record System)整合,生成式人工智能工具的发展和应用得到了极大推动。该系统于2011年启用,旨在作为中央档案馆,集中存放医疗机构的健康记录和数据。
Synapxe 与微软3正在强化生成式人工智能和云计算创新领域的合作。合作的成果之一即医用软件(Secure GPT for Healthcare Professionals)系统,该系统基于 Azure OpenAI服务,旨在构建大型语言模型及相关医疗应用的基础设施,实现任务自动化和高效的信息收集。4这一合作展现出了新加坡政府对生成式人工智能开放和主动的态度及愿与行业领军企业密切合作、推动生成式人工智能在医疗行业的创新应用和建立最佳实践的立场。
日本:多方参与的框架和指导
日本政府在人工智能的监管方面采用了与英美相似的策略,即采用针对特定行业并基于非强制性法规,通过非约束性的行业行为准则来实现管理目标。5
2023年5月,日本成立了人工智能战略专家委员会,重点关注生成式人工智能。在由日本主导的G7广岛峰会期间,生成式人工智能成为重要议题,并贯穿于《G7广岛生成式人工智能进程》报告(G7 Hiroshima Process on Generative Artificial Intelligence)。尽管日本的指导性文件具有非强制属性,但日本政府在人工智能治理方面并未采取被动态度,一些具有普适性和针对特定行业的准则在交通和金融等领域相继实施。6
在医疗领域,日本政府对生成式人工智能所采取的监管方式仍有待完善。尽管尚未发布具体的法规和指导,但日本政府已经明确表示了对人工智能在该行业应用的支持,包括用于药物发现及将软件作为医疗器械使用。
在日本,生成式人工智能工具的应用已经取得了令人瞩目的进展:
- 多款自主研发的生成式人工智能工具已投入使用,用于支持医生的日常事务(例如,生成患者摘要、预测并发症以及追踪处方)。
- 开发Al Fast Doctor应用程序,是一个基于ChatGPT的专门针对日本医疗实践的语言模型LHTM-2,该模型已成功通过日本医学考试,能够通过回答常见问题并协助诊断来为医生提供辅助。7
- CalqKarte是另一款由 ChatGPT 支持的工具,能够在电子病历(EMRs)中记录问诊笔记并按照格式整理,以进一步精简医生的行政性事务。8
由于日本的医院在过去采用技术来精简行政性事务的程度较低,医护人员的工作负担相对较重。因此,整体而言,日本的医疗行业对生成式人工智能工具的需求主要集中在减轻医护人员负担。
此外,日本在2024年将推行职场改革,对医生加班时间设置上限,此举预计也将推动市场对创新技术解决方案的需求增长。
韩国:全面的监管框架
韩国没有专门针对生成式人工智能的法规,但其监管方式与欧盟相似,其提出了一项“人工智能法案”。该法案将各种与人工智能相关的法律整合为一个统一的框架,以对人工智能形成全面监管,并建立道德准则和战略政策路线图。这一方式在某种程度上为生成式人工智能的发展提供了支持。
该方式的一大特点是强调企业自律,而非政府监管。在这方面,政府的唯一角色是提供明确的准则,以确保法律的明确性和对个人的保护。9
在拟议的监管框架下,对“高风险人工智能”的定义仍较为模糊,引发了许多担忧,然而该类人工智能工具已被用于医疗和医疗技术领域。目前尚不清楚这一决定是如何做出的以及哪些人工智能系统应该被归为此类。由于缺乏明确的违规处罚措施,且执行方面也存在不确定性,具体立法变得更加复杂。 一些评论人士担忧,韩国政府的做法可能会阻碍创新,并削弱该国在人工智能国际舞台的竞争力。
尽管如此,韩国蓬勃发展的健康数据生态为创新和开发生成式人工智能工具打下了坚实的基础。据韩国健康保险审查和评估局(Health Insurance Review and Assessment Service)的数据,电子病历系统在韩国的应用非常广泛,普及率极高,是其广泛数字化趋势的一部分,包括临床医学影像的数字化存储、电子医院管理数据库以及远程传感器技术的扩大应用,由此也产生了大量可供访问和分析的患者数据。10
在患者数据隐私和知情同意方面,韩国有着相当严格的法律规定,但在2020年,现有法律有所更新,允许对去除身份信息或使用假名的患者数据进行分享,在促进创新和保护患者隐私之间实现了微妙的平衡。
凭借强大的数据基础设施,注重企业的自我监管以及法律明确性的导向,韩国为人工智能的蓬勃发展奠定了坚实的基础,同时又避免了扼杀国内企业的潜在优势。例如,Naver Health和 Kakao Brain等公司正在积极地与临床机构和大学附属医院合作,促进生成式人工智能与医学实践的融合:
- 截至2023年5月,Naver Health一直在与韩国一家大型眼科诊所合作开发一种多模式聊天机器人,该服务可以通过人工智能视力矫正预测工具对医学影像进行审查,进而提供诊断支持。此外,该公司还计划推出一项“视觉聊天”服务,利用人工智能与电子病历分析患者数据,以实现更加有效的患者沟通和护理。11
- 2022年12月,Kakao Brain与九家大学附属医院达成了联合研究协议,通过开发人工智能模型推动医学影像的进步,该项目旨在研究和开发一项人工智能网络服务来解读胸部X光片,并计划于2024年发布。
中国:可控发展和针对性监管
中国政府正在迅速采取行动开发人工智能技术并对其应用进行监管。在过去两年中,中国政府出台了一系列监管措施,包括2023年7月出台的第一套专门针对生成式人工智能的法规。
德国柏林墨卡托中国研究中心的首席分析师Rebecca Arcesati 表示:“我们需要认识到,中国在生成式人工智能的监管方面已处于领先地位。中国在人工智能监管上迈出了全球范围内最先、也是最雄心勃勃的一步。”
中国政府关于生成式人工智能的过渡性监管措施主要聚焦向公众提供的服务,并有意在创新和合规应用之间达成平衡。122023年7月出台的最终版法规远没有3月首次发布的初稿严格,这反映出政府对行业发展的重视,法规的关键变化包括取消罚款和放弃实名验证要求。此外,这些法规还彰显出中国政府通过相关法规管控人工智能技术发展和促进创新的倾向。但这些法规不适用于企业组织内部生成式人工智能的应用、研究、开发或使用。
同样是针对具体行业制定监管政策,中国却与欧盟有所不同。欧盟偏向于横向监管,寻求涵盖广泛的人工智能领域,13而中国的法规总体上与全球标准保持一致,强调技术关键(例如,训练数据的质量、缓解偏见、知识产权保护和隐私保护等)。然而,中国的监管方针还有一个关键区别,即要求生成式人工智能系统反映“社会主义核心价值观”,这项要求引发了人们对国外生成式人工智能系统(例如,已被禁止的ChatGPT)在中国环境中的稳定性问题以及潜在审查制度的隐忧。这些对全球人工智能的发展都将产生深远影响。
中国政府还采取了一项有效措施——将促进人工智能发展的职责下放到不同的政府部门,让它们完善各自行业的相关监管准则。这一针对具体行业的方针与英国类似,旨在充分利用不同部门的专业知识,制定出能够适应特定行业需求和挑战的监管政策。
尽管国家层面在生成式人工智能上强调增长,地方政府则在监管政策的制定方面发挥着关键作用。某些地方政府采取的措施可能会让生成式人工智能的发展变得复杂。例如,北京市政府制定的相关法规限制生成式人工智能在医疗领域的应用,特别是禁止将其用于自动生成处方。14随着生成式人工智能监管政策的演变,企业不仅需要密切关注国家层面的监管政策,还需要密切关注省级和市级政策法规的变化,这些政策法规都可能会影响生成式人工智能在医疗健康行业中的应用可行性和投资,从而影响行业的整体发展。
在医疗健康领域,面向公众的生成式人工智能应用是重点监管对象。按照这个逻辑,监管机构下一步将重点对面向非患者的人工智能应用进行监管(例如,用于减轻医务人员工作负担的诊断聊天机器人或沟通工具)。根据同行审评、开源的医学期刊BMJ Open的数据,中国面临医生短缺的问题,人均医生数量仅在全球排名第77,城乡医疗差距也很明显。平安好医生等生成式人工智能工具则能够辅助医生进行问诊,15而MedGPT(一个先进的聊天机器人和医疗文档平台)16能够在缩小城乡医疗差距方面发挥重要作用。这些创新缓解了长期以来因患者数量增加而导致的医生负担加重的问题。
对医疗行业和生成式人工智能公司的启示
生成式人工智能领域发展迅猛,相关监管制定正在迎头赶上,但政策框架仍有待完善。然而,这对生成式人工智能和医疗行业参与者而言不失为一个好机会,行业参与者可借此获取一线经验,制定生成式人工智能愿景,并对监管机构的态度产生积极的影响。
为了实现这一点,相关企业首先应针对生成式人工智能的应用制定内部愿景和管理架构,确保与企业的战略目标相一致。其次,企业可以战略性地在不同应用领域落地小规模的试点项目,从中获取宝贵经验,了解与不同用例相关的风险和收益,从而降低监管风险。此外,企业还可以通过与其他行业参与者或组织合作或联盟,形成合力,促成共识,并积极影响监管政策的制定。
L.E.K. Consulting是L.E.K. Consulting LLC的注册商标。本文档中提及的所有其他产品和品牌均为其各自所有者的财产。
© 2024 L.E.K. Consulting
尾注
1Tan K., Strait Times, 2023
2Chiang, S., CNBC, June 2023
3Frontier Enterprise, July 2023
4Abdullah, Strait Times, 2023
5Nussey, S., Kelly, T., Reuters, July 2023
6Habuka, H., CSIS, February 2023
7Fast Doctor Co. Ltd., PR Times, 2023
8KandaQuantum Inc., PR Times, 2023
9Yulchon LLC, March 2023
10Digital Health South Korea, Intralinks, 2019
11ETNews, May 2023
12Wu, Y., China Briefing, July 2023
13Wu, Y., China Briefing, October 2022
14South China Morning Post, August 2023
15Shenshen Z., Shine, 2023
16MedCloud.PH, MedGPT, 2023