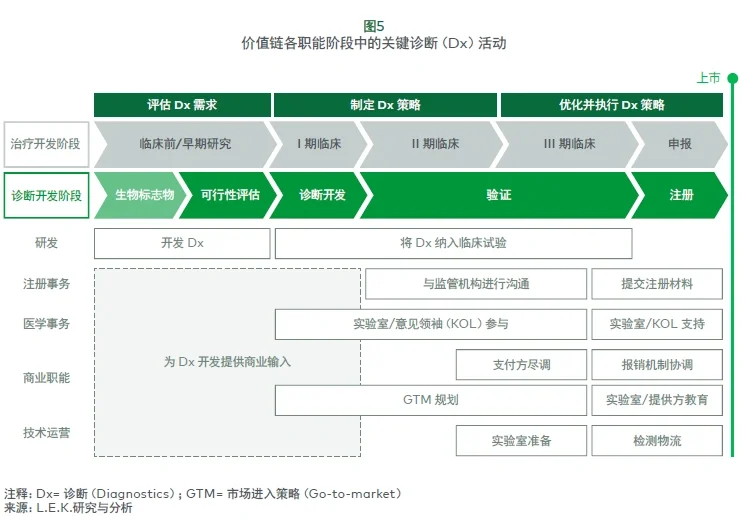
例如,实验室自建检测(LDTs)可能在报销方面面临难题,并且需要广泛的实验室验证,但在美国,它们通常能够更快上市,并支持更多且更复杂的生物标志物,因为不需要获得监管批准。相比之下,体外诊断产品(IVD kits)则受到 FDA 监管,无法覆盖所有检测靶标,并面临来自其他诊断产品的更激烈竞争,但其优势在于任何配备相应仪器的 CLIA 认证实验室都能开展检测,且通常享有更高的报销比例。对于一些公司而言,同时推进并支持同一诊断产品的 LDT 和 IVD 两种版本,将进一步增加运营复杂性,并需要额外的上市准备工作和资源投入。
4. 建立独立的诊断上市策略
精准医学领域的领先企业通常将 Dx 上市和治疗产品上市视为既相互关联又彼此独立的流程,两者涉及的利益相关方和挑战各不相同。由于 CDx 的关键利益相关方群体高度多样,且与治疗产品的利益相关方几乎没有重叠——例如病理科医生与开具处方的肿瘤科医生——因此,有针对性的推广是提升认知度和处方意愿的最佳方式。鉴于有效检测(尤其是新型 CDx)的复杂性,有效的上市策略应涵盖对所需仪器或其他技术的考虑,兼顾实验室操作需求(如 LDT 支持、样本处理指导等),同时也要将市场准入因素纳入规划之中。
理想状态下,企业在制定上市计划时,应同时考虑 Dx 与治疗产品上市策略之间的相互作用。例如,在精准医学环境下,基于用药患者数的传统销售激励模式可能并不适用;相反,被筛查的患者数量可能是更有意义的指标。制定专门的 Dx 上市策略,有助于推动更广泛的市场应用,并扩大精准医学的整体商业潜力。
5. 在构建内部能力的同时,有针对性地利用合作伙伴的专业资源
在借助内部与外部关键合作伙伴的专业能力来开发、申报和生产 Dx 检测的过程中,生物制药公司应有针对性地扩展特定活动,并确保具备足够的监管能力。根据企业规模与能力的不同,某些任务可能超出内部能力范围,例如:生物标志物的选择、检测开发、研究结果解读或 Dx 产品的销售等。另一方面,那些需要与治疗团队密切协作的活动(如样本采集与保存),或具备战略意义的任务(如市场准入),则更适合由企业内部直接管理。
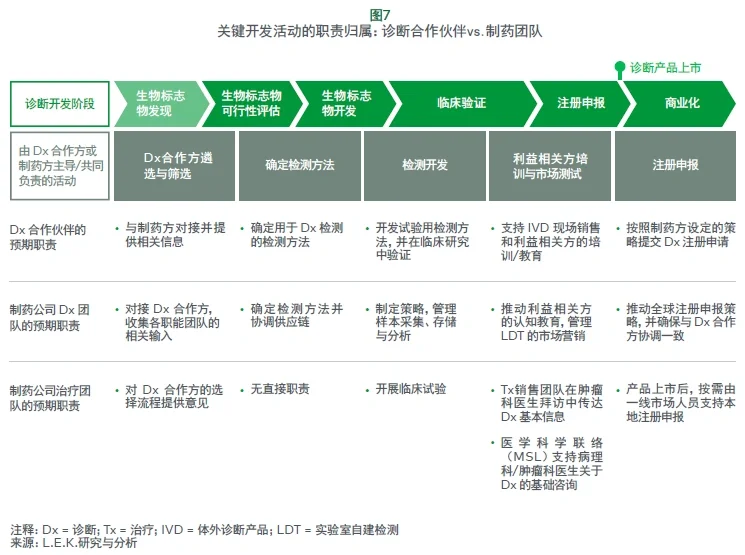
即便借助合作伙伴,Dx 上市仍需要在整个价值链中配备具备 Dx 专业知识的内部专职资源。既了解 Dx 又熟悉精准医学治疗的复合型人才十分稀缺且需求旺盛,因此企业需要及早规划,并制定强有力的人才留存措施。在外部专业知识与内部核心知识之间找到平衡至关重要,以便有效监督 Dx 合作伙伴;这些外部伙伴可能缺乏企业内部的整体视角,也未必有足够动力去持续优化检测或充分投入上市相关工作(见图7)。