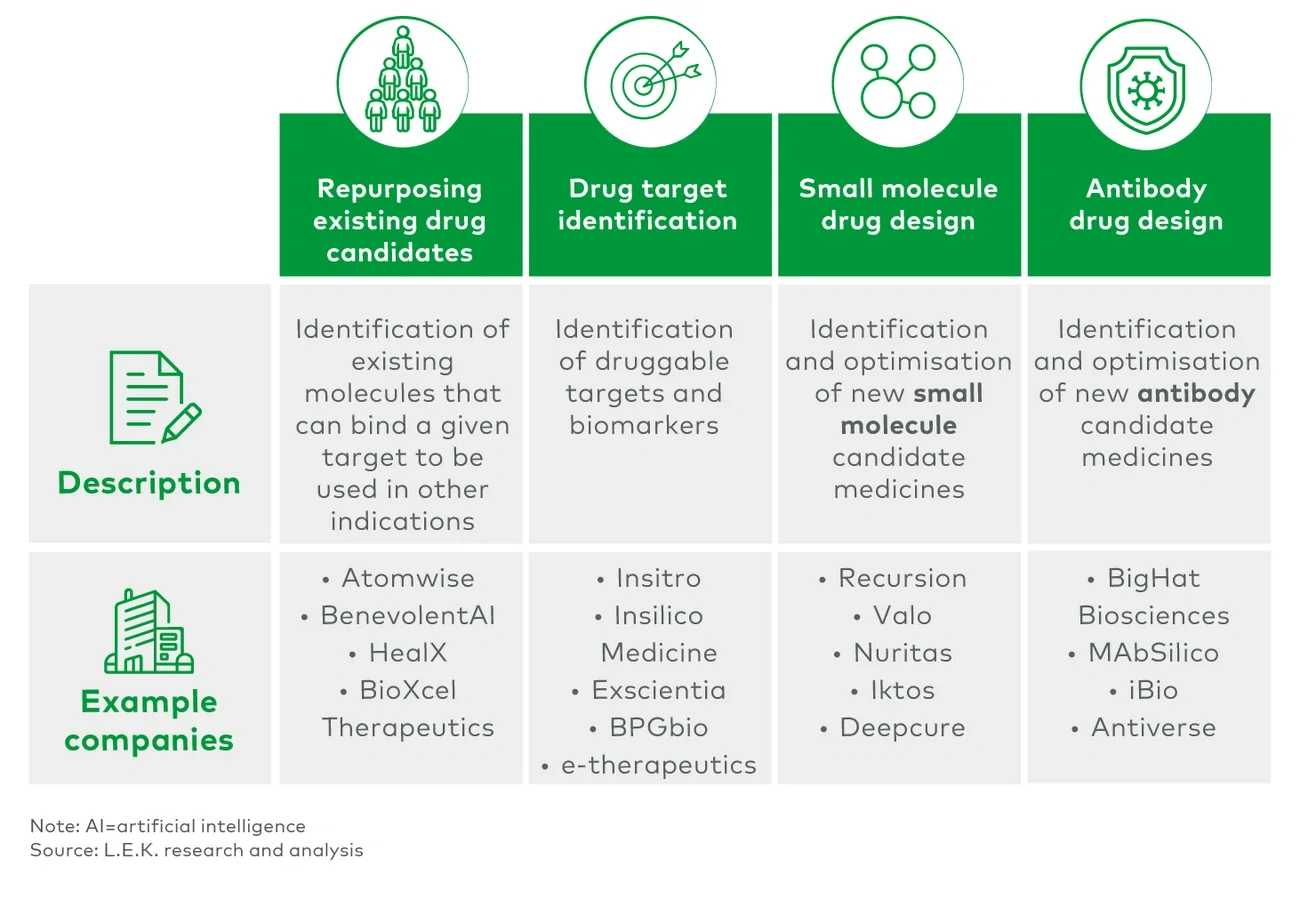
1. 现有候选药物的再利用
在药物发现领域, 人工智能在现有候选药物的再利用方面展现出了巨大潜力,人工智能能够快速识别已知药物的新适应症,从而实现老药新用。目前,已有超过250家公司正在通过人工智能技术在这一领域展开探索,特别是在新冠疫情的推动下,这种快速且灵活的药物发现方法更是迎来新机遇。
以Baricitinib为例,这款原本用于治疗类风湿性关节炎的Janus激酶抑制剂,在BenevolentAI的知识图谱平台辅助下,被成功识别为治疗新冠的潜在药物。该药物于2020年获得美国食品药品监督管理局(FDA)的紧急使用授权,用于治疗住院的新冠患者,并在2022年基于四项随机临床试验的积极结果获得了全面批准。
通过这种方式发现的大多数化合物仍处于临床试验阶段,但这一领域的前景依然被普遍看好。随着数据资源的丰富和开放,数据的可用性和质量都有望持续提升,为人工智能在药物再利用领域的深入应用提供坚实基础。
2. 药物靶点识别
人工智能技术能够快速构建分子疾病模型,并在识别药物靶点和生物标志物方面展现出比传统方法更高的效率。面对海量的生物医学数据,整合多样化的非结构化数据集将是一项艰巨的任务,但人工智能却能对这种非结构化的数据集进行有效提取和分析(例如,期刊文章和组学数据库,以及医学影像和真实世界患者数据)。知识图谱将能够揭示实体之间的新联系,然而这一过程将高度依赖数据集的标准化和标注质量。
目前,利用人工智能进行药物靶点识别的项目已经通过了药物发现和临床前开发阶段,至少有20种由人工智能识别出的具有新型疾病-靶点关联的药物正在进行临床一期和二期研究。随着企业不断扩充数据集,并将研究成果反哺给人工智能算法,预计未来将有更多具有新型疾病-靶点关联或全新靶点的药物涌现。
3. 小分子药物设计
利用现有的化学结构数据,人工智能能够迅速模拟复杂的化学性质,并在药物结构设计上展现出比传统方法更高的速度和准确性。在此应用场景中,企业可借助人工智能对现有的化学库进行筛选,或生成新的化学结构设计。然而,数据的可用性和易用性仍然是该领域的关键挑战,因为与数十亿种化合物的完整化学空间相比,训练集规模相对较小。
此外,不同靶点类别的数据的丰富程度也存在差异(其中,激酶和G蛋白偶联受体的数据最为详尽),这在一定程度上限制了通用模型的构建以及候选药物的创新性。
如今,人工智能工具已成为小分子药物设计流程中不可或缺的一部分,而更大规模的预测性解决方案也正在不断迭代优化。目前,相较于人工智能设计的抗体药物,人工智能设计的小分子药物更为普遍。Exscientia和Insilico Medicine等公司正在引领人工智能设计小分子药物的第一波浪潮,这些公司的临床项目已进入二期试验阶段,其结果有望揭示该人工智能在该应用场景下的成熟度和未来潜力。
4. 抗体药物设计
在抗体药物设计领域,人工智能正展现出日益增长的潜力,包括对现有结构的优化,以及从头开始的候选药物设计。尽管前景广阔,目前仅有少数人工智能设计的抗体药物进入临床阶段。抗体分子的复杂性为设计过程带来了独特挑战,如需要更强大的计算能力来运行大型模型。抗体序列和抗体-抗原对数据的稀缺性也限制了人工智能模型的发展。此外,由于多数训练数据都源于传统抗体设计方法的数据库,因此如何平衡抗体的特异性和亲和力等传统挑战依然存在。
幸运地是,专注于人工智能抗体药物设计的研究团队和企业生态正在不断扩张。过去一年中,多家大型制药公司纷纷宣布其内部的创新成果或与初创企业或科技巨头展开合作。
最新动态中,Xaira Therapeutics成功筹集超10亿美元资金,初期将专注于从头设计全新抗体。该公司汇聚了具有蛋白质和抗体设计扩散模型设计经验的科研人员,以及基因组学和蛋白质组学团队。未来,随着人工智能平台与制药公司合作的深化,以及标准化、开源数据的不断增加,人工智能在抗体药物设计领域的成熟度将进一步提升。
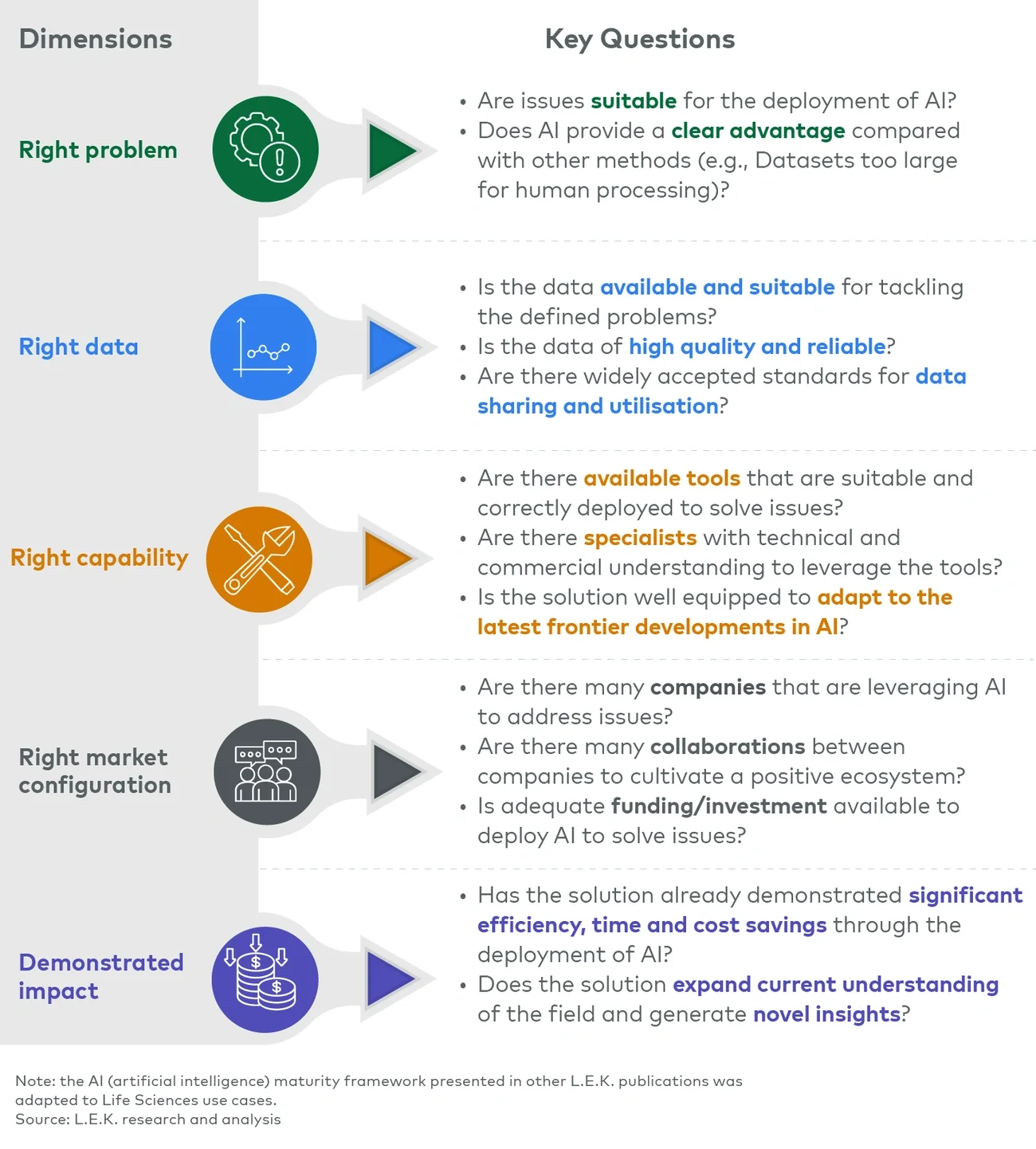
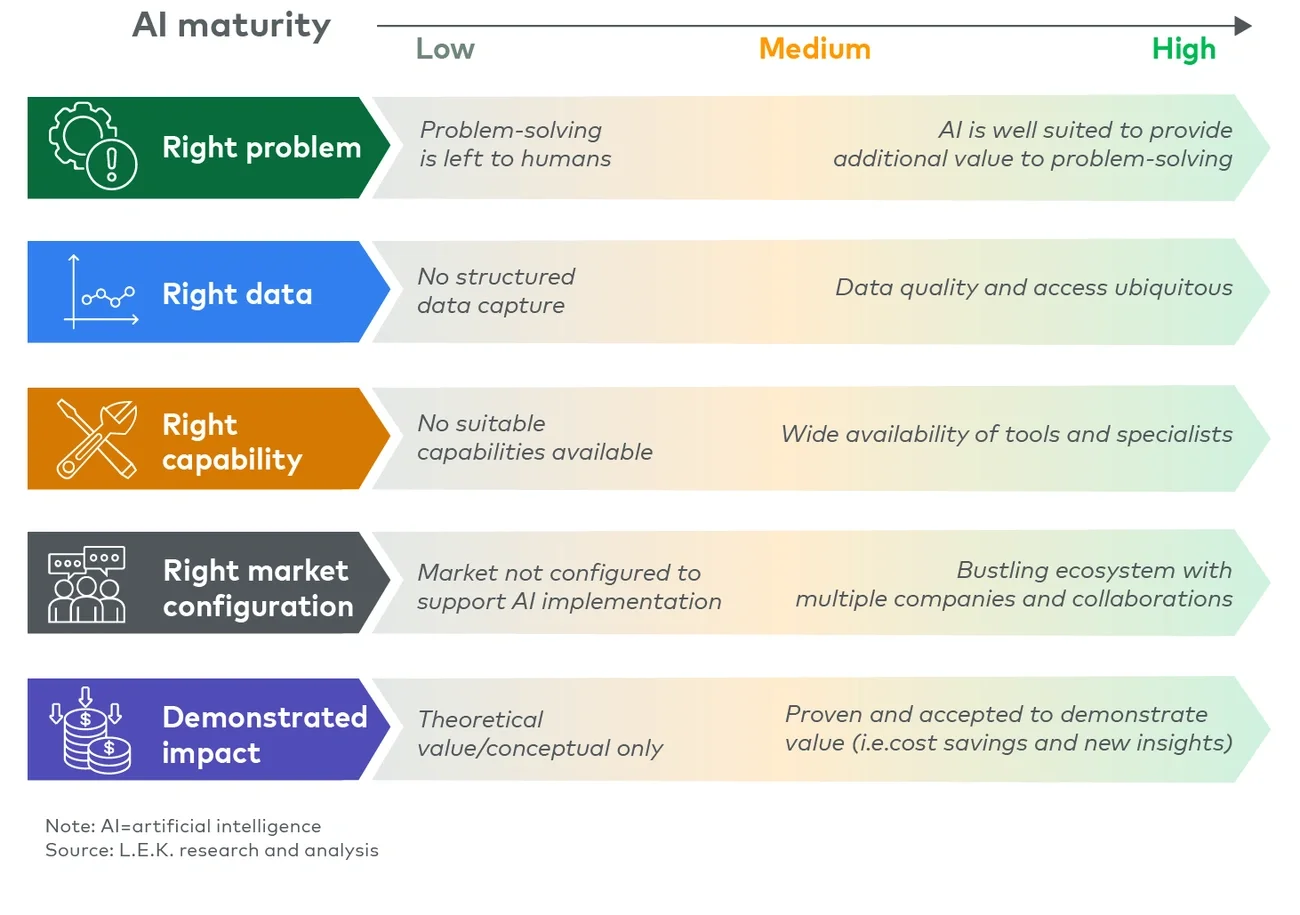
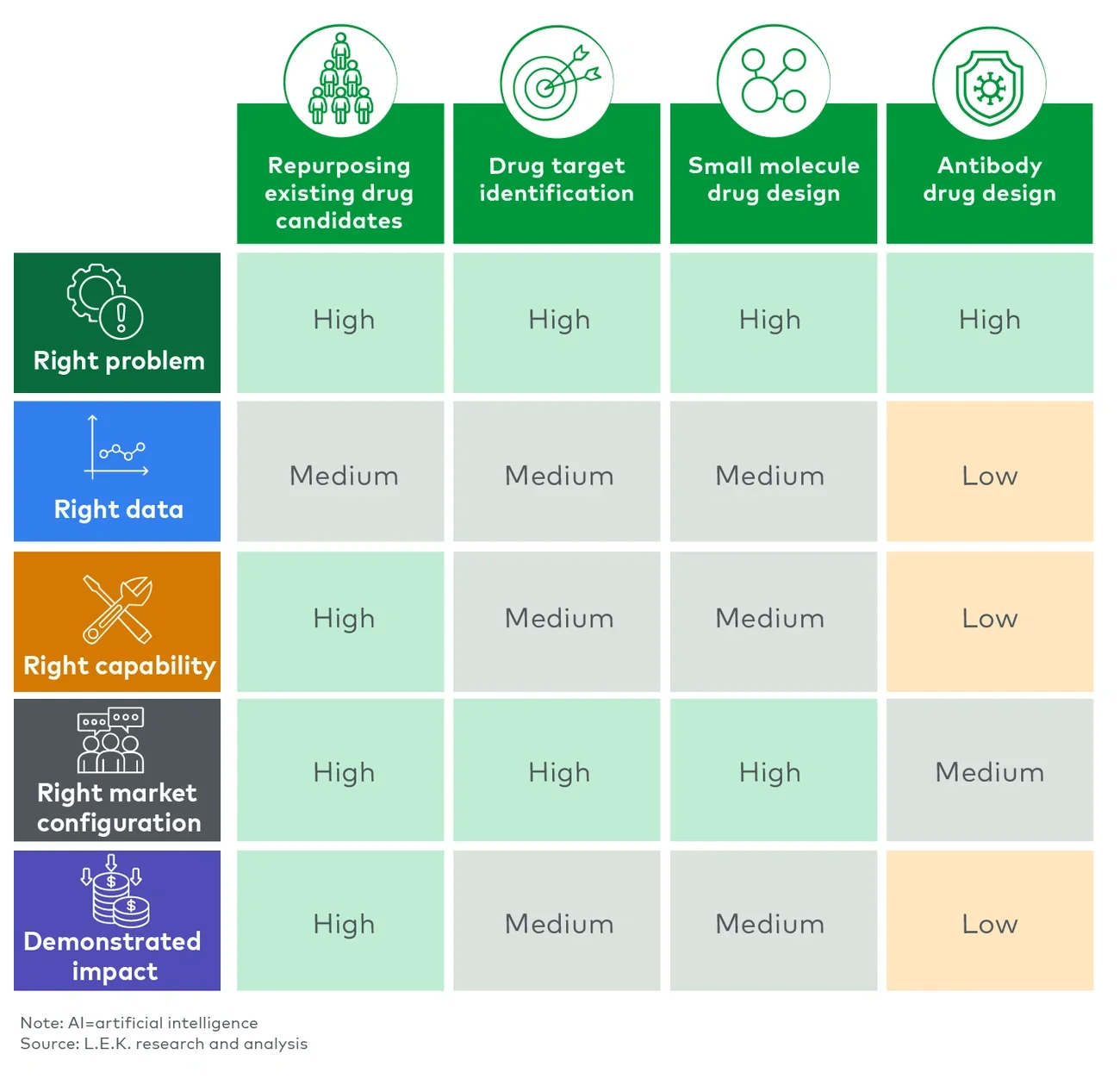
展望:人工智能在不同应用场景中的成熟度
在生命科学领域,人工智能应用的成熟度呈现多样化趋势,且因应用场景而异(图4)。在现有候选药物再利用和靶点识别等方面,人工智能应用已经取得了显著进展,然而在抗体药物设计等其他领域,人工智能应用仍处于较为初级的阶段。