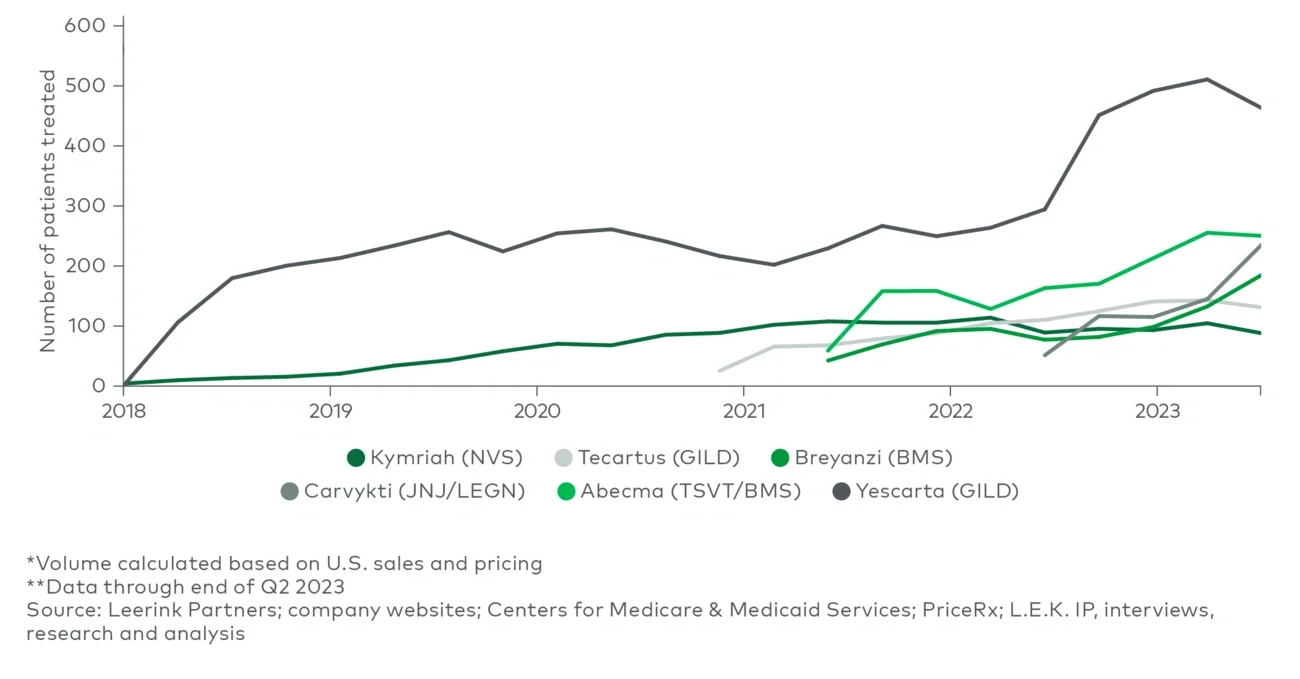
- 最小化对非目标组织或细胞的影响:细胞因子释放综合征(CRS)是细胞疗法最常见的不良事件之一。 当前已上市的细胞疗法靶向的是单一抗原,不同批次的产品存在一定差异(例如,T细胞的效力和持久性存在差异),这可能会引发免疫系统的连锁反应,或因毒性反应限制治疗剂量。目前,托珠单抗(tocilizumab)等免疫抑制剂可用于治疗CRS,而下一代细胞疗法(例如,采用新细胞类型的疗法、更加精准的靶向治疗方法)旨在最大程度地减少CRS的发生。从实际效果来看,相较于老一代CAR-T疗法(例如,Kymriah和Yescarta),最近获批的药物(例如,Breyanzi)的确表现出更低的CRS患病率。
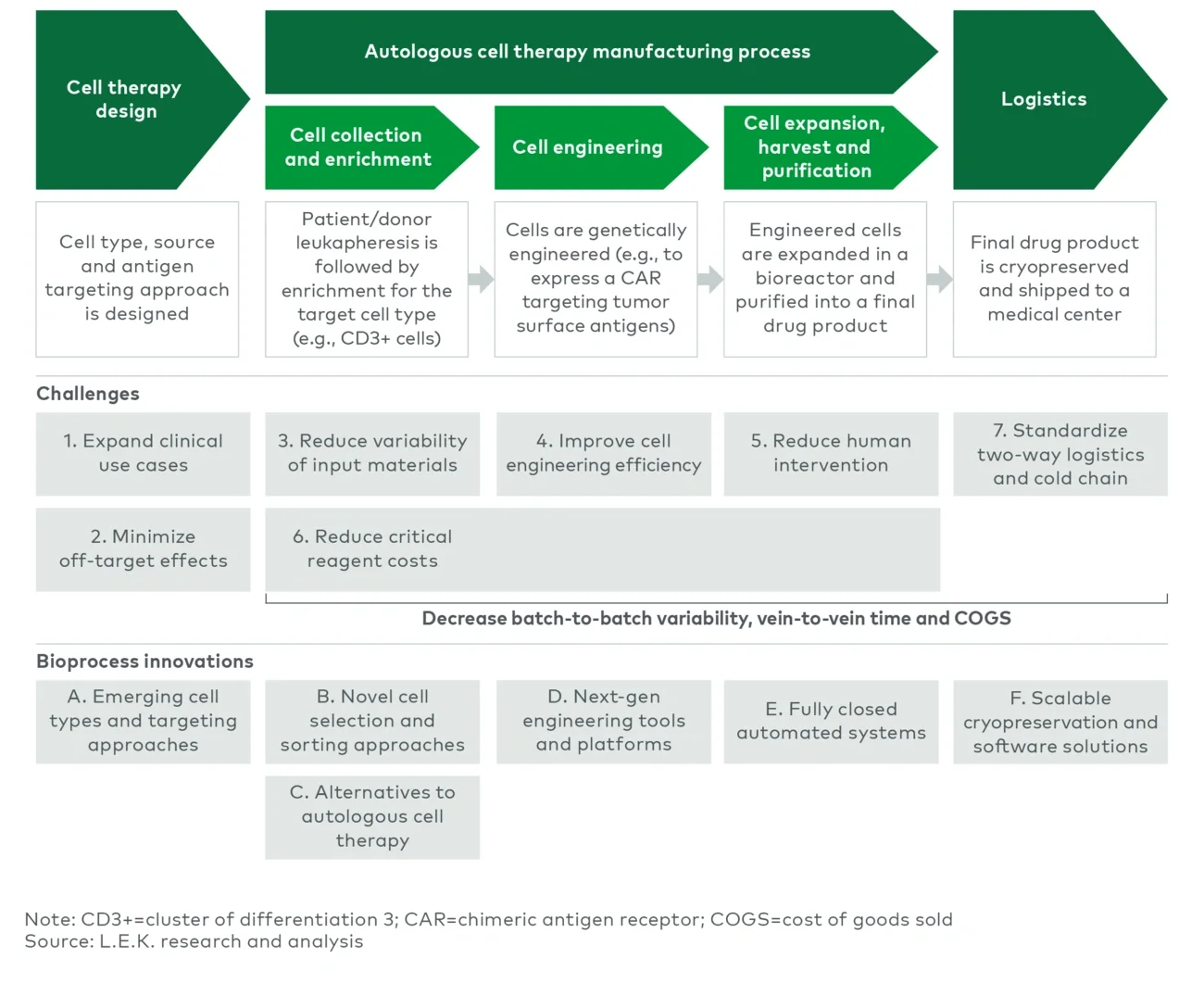
生产过程中的挑战
缩短从采集细胞到回输至患者体内的时间、降低生产成本以及减少不同批次之间的差异是个性化细胞疗法所面临的核心挑战。目前,商业化自体细胞疗法一次完整的治疗周期为三到五周,治疗周期较长的主要原因在于需要将患者的细胞运往生产地,生产过程较长且批次失败率较高(可能会超过10%),还需要协调最终产品的交付。在某些情况下,治疗周期拉长意味着患者可能需要进行过渡性治疗,这可能会导致患者的毒性反应和并发症增加,最终降低细胞疗法的有效性。
提高生产效率是缩短治疗周期的关键,一方面需要缩短整体的生产时间,另一方面需要避免因人为失误和污染导致的批次差异,以降低失败率。从经济效益和患者健康的角度来看,失败率高不仅会导致成本高企,还有可能会导致产品延期上市(强生和传奇生物的Carvykti曾因产能问题在英国延期上市)。已经上市的CAR-T产品可能需要好几年才能改进生产工艺并降低失败率,因为优化生产工艺时一般使用的是非疾病状态的材料。
- 降低生产原料的差异性:由于自体细胞疗法的本质特征,患者的健康状况、预处理程度、相关淋巴细胞水平、从患者体内提取的细胞数量限制(即单采率)都可能会导致生产原料出现显著差异。此外,单采设备相关因素(例如,采集流程和设备、冷冻设备、人员经验)也会导致生产原料出现较大差异,从而导致不同生产批次的品质不稳定。血液和生物治疗促进协会(Association for the Advancement of Blood and Biotherapies)、细胞治疗认证基金会(Foundation for the Accreditation of Cellular Therapy)等组织正在着手制定工作流程标准(例如,单采、产品标签)。此外,在已经上市的第一代细胞疗法的基础上进行生产流程的优化至关重要。这些做法能够极大推动未来自体细胞疗法的成功,随着细胞疗法的目标患者群体越来越大,生物制药企业可能还需要在更广泛的地区建立新的单采或生产设施。
- 提高细胞工程效率:目前工程化T细胞主要通过病毒载体制备,即利用慢病毒(例如, Kymriah)或γ逆转录病毒(例如,Yescarta)将CAR插入到靶细胞中。更多使用病毒转导的原因在于,常见的低成本化学转染方法,包括病毒载体生产中用于细胞系转染的方法(例如,聚乙烯亚胺、脂质体转染胺),在免疫细胞中的转染效率较低。以病毒载体为基础的方法的进步(例如,Penn Medicine的24小时临床前CAR-T生产工艺)有望提升细胞工程效率,并进一步改善细胞疗法的有效性(即细胞扩增需求降低,可能会改善工程化细胞的质量)。然而,病毒载体仍然是影响销货成本的一个重要因素,也是导致供应链更加复杂的因素。例如,慢病毒成本可占生产一个批次的总成本的10%-25%6,7,因为慢病毒制备所需的质粒DNA成本昂贵,慢病毒的质量也不稳定,且产量较低。慢病毒供应受限甚至可能会让药物的生产陷入瓶颈(例如,百时美施贵宝在Breyanzi 生产中遇到的慢病毒供应挑战)。
不以病毒为载体的细胞工程方法也已经出现。例如,利用仪器设备进行转染(例如,电转染)已成为一种可行的替代方案,但仍然面临一系列关键挑战,其中包括由于外界条件对细胞造成的压力而导致细胞活性较低。鉴于每个批次的细胞治疗产品都是根据患者个体特征定制的,并且每次单采的细胞数量有限,这一挑战尤为令人担忧。另外,该类方法在扩增时间(例如,细胞倍增时间)以及大规模生产方面也面临挑战(如果采用电转染方式,细胞扩增之前还需要进行额外的操作)。 - 减少人为干预:相较于成熟的生产流程(例如,单克隆抗体的生产流程),当前的细胞疗法生产过程需要更多人为干预。现有的细胞治疗设备遵循模块化的方法,主要侧重于单项操作(例如,转导/转染、细胞激活、细胞扩增、灌注/完成),以及部分需要经过培训的人员手动转移的操作,这些工作都进一步推高了劳动力成本。目前,越来越多生物制药企业选择采用目标导向的一次性闭环系统,以精简生产流程,同时降低污染风险(例如,美国FDA最近就Kymriah的生产工艺问题向诺华发布了无标题信)。目前,大规模量产中使用最多的细胞扩增系统是Cytiva公司的Xuri系统,但未来有可能会被多功能(例如,筛选、激活、扩增)全自动系统所取代(例如,被广泛采用的Miltenyi Prodigy系统,或Lonza的封闭全自动系统Cocoon)。
尽管上述解决方案能够简化生产流程,但劳动力仍然是影响生产成本的关键因素,占每批次总成本的25%-50%6,7,具体取决于开发阶段、设备的模块化程度以及生产流程的自动化水平。模块化的设备也需要手动操作进行衔接,这增加了污染或出现人为失误的风险。此外,当前的加工设备已经针对CAR-T细胞进行了优化,但通常无法灵活地针对其他细胞类型进行优化(例如,自然杀伤细胞在细胞扩增过程中可能需要更大的体积)。 - 降低关键试剂成本:自体细胞疗法的生产需要对关键原料(例如,CD4或CD8筛选)进行均质化处理,因此需要一些额外步骤(例如,细胞激活),从而导致成本上升、生产时间延长。
细胞疗法的生产过程中,T细胞激活至关重要,最流行的细胞分选方法是磁珠细胞分选(MACS) 或荧光激活细胞分选(FACS)。目前,磁珠细胞分选(例如,Miltenyi的MACS、赛默飞的 Dynabeads)是晚期临床研究和商业化产品生产的首选方法,但同时也是导致成本增加的重要因素,每次分选的成本超过5,000美元7(占每批次产品生产总成本的5%-10%7)。如果细胞分选过程中需要同时使用多个标记物,连续的分选步骤以及相应的磁珠需求将进一步推高成本。此外,可能还需要其他(通常是手动的)步骤来降低残留物水平,以达到临床质量标准,这些都会导致成本增加、生产周期延长。FACS是磁珠分选的替代方案,这种分选方法的自由度更高,能根据表面标记分离细胞,但其通量有限,良好生产规范(GMP)选择较少,并且需要经验丰富的全职人员进行操作,这些因素限制了FACS在大批量细胞分选中的使用。
除了磁珠,免疫细胞的制备还高度依赖一些特殊耗材(例如,细胞因子)和符合GMP规范的培养基,这些也是导致成本增加的重要因素,尤其在早期开发阶段,生产需要一定程度的定制材料,但由于疗法尚未实现规模量产,供应商难以通过规模经济大量盈利,因此其定制材料的价格通常较为高昂。 - 标准化双向物流和冷链:自体细胞疗法的生产不同于传统的中心化生产模式,患者的细胞必须经历从医疗中心(例如,单采设备)收集、运输到中心化生产设施、制成药品、送至患者手中这一系列环节。为了满足商业化的需求,试点规模的工艺流程被迅速采用,然而低温保存、身份链(COI)和监管链(COC)等解决方案并未针对大规模生产进行优化。
目前,大多数低温保存都要用到液氮,然而这种方式难以维持均匀的温度,并且在大规模应用和可持续性(例如,液氮的批量存储和运输)方面面临挑战。随着生产需求的增加,这些挑战可能会被进一步放大。液氮还会因气体释放带来污染风险,因此在符合GMP规范的设施中,这种类型的冷冻方式通常无法使用。此外,在运输过程中,由于生化毒性和渗透压造成的细胞损失与冷冻前后的暴露时间高度相关,产品质量可能会因在冷冻前长时间接触细胞冷冻介质(例如,二甲亚砜)而受到负面影响。
身份链和监管链流程尚未标准化,向电子系统和电子批次记录的过渡可能会出现断层。例如,审计记录涉及纸质文件以及多个电子平台,开发人员、CDMO、医疗中心等不同相关方可能会面临软件不兼容的挑战,以及不同地区的监管要求(例如,法国的数据存储规则更为严格)。
生物工艺创新
L.E.K.总结出六个最有潜力解决上述挑战并改进细胞疗法的生物工艺创新:
- 新的细胞类型和靶向方法
- 新的细胞筛选和分选方式
- 自体细胞疗法的替代疗法
- 下一代细胞工程工具和平台
- 全封闭自动化系统
- 可大规模使用的冷冻保存和软件解决方案
- 新的细胞类型和靶向方法:为了让细胞疗法能够进一步用于非实体瘤的治疗,生物制药企业正在探索新的细胞类型和能够提高细胞疗法持久性的靶向方法与机制。本报告未对所有细胞疗法相关创新展开详尽讨论,仅聚焦于部分重点领域。
目前,科学研究界对工程化T细胞的了解最为透彻。此外,针对自然杀伤细胞(NK)、肿瘤浸润淋巴细胞(TIL)、树突状细胞、巨噬细胞的其他免疫细胞类型的研究也正在进行中,旨在探索它们是否具备改善临床疗效和安全性的潜力。例如,NK细胞在降低毒副作用以及治疗浸润实体瘤方面展现出一定潜力,但仍需要克服治疗效果不够持久的挑战;TIL细胞针对的是患者自身的肿瘤细胞,具有高度特异性,并能够大量扩增,允许患者重新用药。值得注意的是,与当前其他T细胞衍生疗法相比,使用新的细胞类型的细胞疗法对生物工艺有着不同的要求(例如,培养密度、试剂、培养天数、激活过程等)。
除了新的细胞类型,双重靶向等新机制也有助于解决实体瘤的异质性问题,同时可利用替代受体(例如,T细胞受体)更广泛地选择可靶向抗原(即通过提高敏感性和与生理信号的耦合,改进对肿瘤细胞的检测和杀伤)。此外,对其他机制的探索也在进行中,以更好地渗透肿瘤微环境(例如,装甲细胞)和避免出现不良的免疫反应(例如,隐形细胞),并最终能够靶向难以治疗的肿瘤,同时改善药物的持久性和效力。
这些创新能够充分释放细胞疗法的治疗潜力,但也可能导致第一波CAR-T疗法所采用的生物工艺遭遇挑战或变化(例如,NK和TIL细胞扩增需要更大容量,而当前所使用的设备并不能很好地满足这一生产需求)。 - 新的细胞筛选和分选方式:市场中既有根据标记(例如,MACS、FACS)进行细胞分选的方式,也有不采用标记的分选方式。相较于传统的MACS和FACS,新的根据标记进行细胞分选的技术(例如,Cellular Highway的涡流驱动细胞分选技术,Akadeum的浮力激活细胞分选技术)旨在克服成本高、通量有限以及细胞损失量大等方面的挑战。然而,这些新技术是否能用于规模生产仍有待验证。
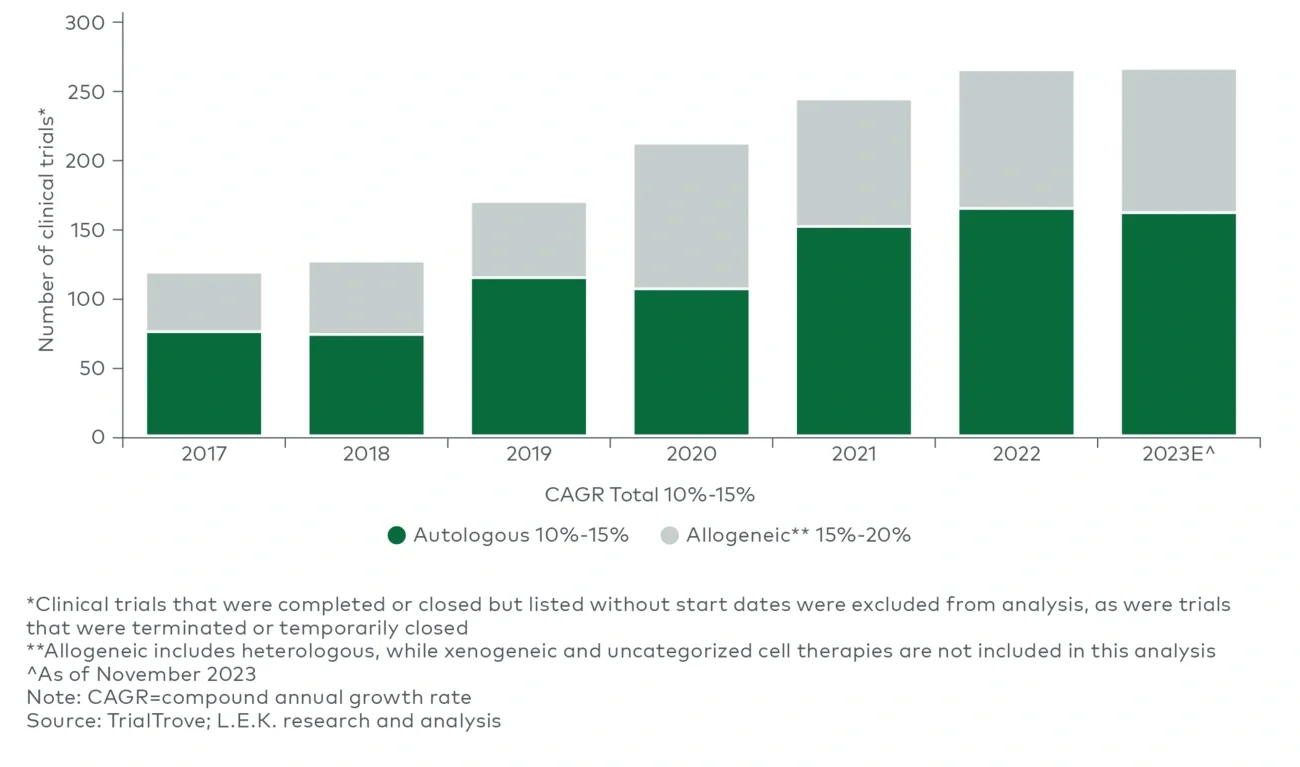
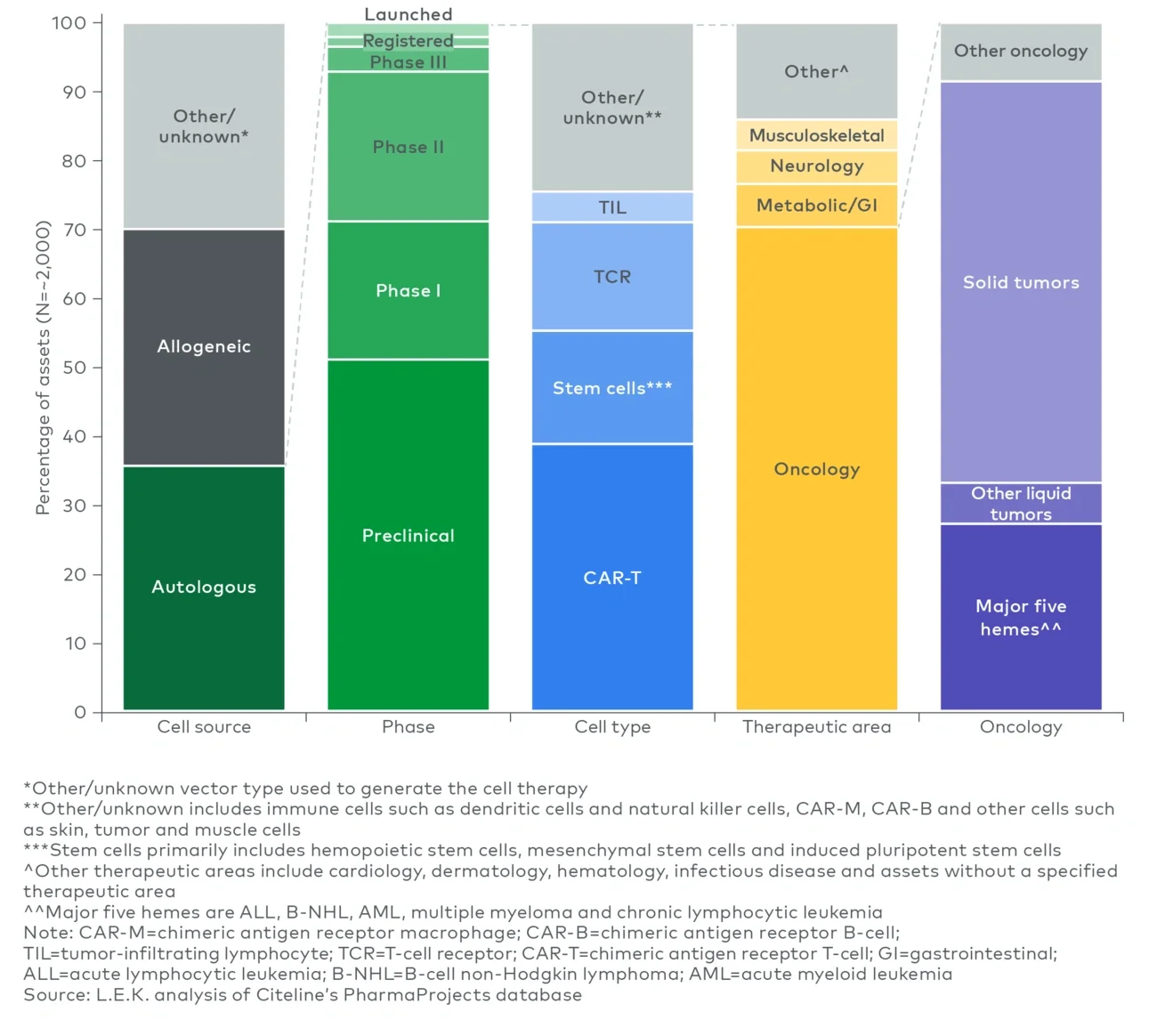
新的不采用标记的细胞分选技术已成为批量分离和精细化筛选细胞的替代方式,这类方式能够避免不必要的细胞激活,降低最终药物产品的试剂(例如,磁珠)污染风险,并有可能在不增加成本的情况下增加标记的数量和多样性(例如,在传统方式下,使用两个标记进行分选会导致磁珠相关成本翻倍)。其中有一种新的基于物理特性(例如,尺寸、密度、可压缩性)进行细胞分选的方法,例如,Aenitis、Draper 和 FloDesign Sonics 等公司的超声波(声流体)细胞分选技术,以及Curate Bioscience和Cytonome等公司的微流控细胞分选技术。ThinkCyt是一家专注于研发的生物技术公司,该公司正在使用计算机模拟的方法将非物理“标记”与流式细胞术相结合,根据表型(例如,激活与静止)进行细胞分选。如果最终可行,该技术将为其他用于大规模细胞分选的计算机模拟方法铺平道路。 - 自体细胞疗法的替代方案:尽管业界非常关注自体细胞疗法的进展(占细胞疗法临床管线的35%-40%3),但其他新兴疗法(例如,同种异体细胞疗法、体内基因治疗)也极具潜力,并能够避免体外细胞疗法在生物工艺方面所面临的诸多挑战。鉴于自体细胞疗法已经展现出卓越的疗效和持久性,即使这些替代疗法开发成功,可能也无法完全取代自体细胞疗法,而是与之共存。由于生产过程存在巨大差异(例如,同种异体细胞疗法采用的是传统的生物制剂的规模化生产方式),这些疗法面临着一系列完全不同的挑战,例如,同种异体细胞疗法主要需要解决细胞供体管理、移植细胞的持久性以及免疫排斥等方面的挑战,体内基因疗法则在针对特定细胞进行转染以及基因编辑脱靶等方面面临风险。此外,目前用于生产自体T细胞疗法的工具和工艺无法直接适用于同种异体细胞疗法,两者需要不同的生产流程、基础设施以及流程解决方案。
- 下一代细胞工程工具和平台:相较于以病毒为载体的转染方法和传统的电转染方法,下一代转染平台旨在降低生产成本(例如,无需昂贵的慢病毒),改善与其他细胞工程方法的兼容性(例如,CRISPR、转座酶),提高规模化生产能力,并提升编辑后的细胞活性。
流式电转染平台(其中包括来自MaxCyte、Kytopen和Draper的平台)在传统电转染方式的基础上进行了升级,旨在缩短处理时间,并最大程度地解决大规模生产和细胞活性方面的问题。最近,Vertex的镰状细胞基因疗法 exa-cel获批上市,这一事件对MaxCyte的ExPERT平台而言是一个重要的监管里程碑,这也为FDA接受非病毒细胞工程替代疗法创立了先例。CellFE、Avectas以及SQZ Biotech 等其他玩家采用的是基于微流体的机械方法(例如,快速的细胞压缩或膨胀),这种方法能够降对耗材的需求(例如,缓冲液),同时提高转染效率以及细胞的回收率和存活率,还能释放更脆弱且更难以改造的细胞(例如,NK细胞)的治疗潜力,并缩短扩增时间以及最终的治疗周期。 - 全封闭自动化系统:第一代细胞疗法的生产依赖于彼此独立的设备和操作,且需要操作人员手动将材料转移至下一个环节。目前,生物制药企业正在越来越多地通过模块化产品生态系统(例如,赛默飞的细胞治疗系统产品线)将关键的操作环节进行整合和自动化,然而真正独立的全封闭自动化系统仍然凤毛麟角。
下一批细胞疗法的生物工艺设备旨在实现中心化和多线并行(例如,在同一洁净室中处理多个患者的药物)的生产模式,并通过解决开放式系统的污染(和交叉污染)风险、对有经验的操作人员的高度依赖以及批次差异等一系列关键问题,来为去中心化生产铺平道路。
除了Lonza的Cocoon系统,Adva和Ori Biotech等公司也正在开发一体化的符合GMP规范的解决方案,这些解决方案整合了多个工作流,并形成了一个全封闭的自动化系统,能够实现中心化的并行操作和即时生产。Xcellbio公司的AVATAR Foundry平台能够自动进行液体处理以简化单元操作,该公司目标通过在细胞转导和扩增过程中进行代谢调节来提高最终细胞疗法的功效。此外,Cellares公司也专注于其Cell Shuttle生产平台的开发,该平台采用了预组装的全自动生产舱,符合ISO 8级别的洁净度标准,并能够同时处理16个批次的细胞治疗产品。MultiplyLabs公司和Cellular Origins公司则正在增强其现有的生产和质量控制测试方法,利用机械臂对市场领先的设备(例如,Cytiva 公司的Xuri细胞扩增系统)进行单元操作,以减少对生产流程的重大变更和重新验证。
生产设备在技术方面的进步能够加速实现去中心化生产,甚至实现床旁生产(POC),即在医疗中心等非传统GMP 环境中进行生产。FDA药物评价和研究中心一直以来都非常关注POC生产策略,然而这种生产模式也会带来一系列挑战,例如:不同生产地点之间的差异以及产品分析方面的差异,这些因素可能进一步增加对生产过程中的分析测试解决方案的需求。 - 可大规模使用的冷冻保存和软件解决方案:目前市场上无需使用液氮的冷冻保存方式较为有限,其中最引人注目的是Cytiva的控速降温仪(VIA Freeze)和超低温运输系统(VIA Capsule)。然而,由于电力成本以及备用电源系统的成本非常高,无需液氮的冷冻保存方案在经济效益方面仍然面临着一定的挑战。除了关注冷冻和解冻的过程,Cryoport Systems、BioLife Solutions以及CSafe 等其他的解决方案供应商正在致力于开发端到端的冷冻保存解决方案,以简化生产流程。然而从更广泛的角度来看,完全封闭的自动化系统可能才是长期可持续的冷冻保存解决方案,这些系统既能够被大规模使用,满足自体细胞疗法的POC生产需求,同时降低对传统的冷冻保存方式的依赖程度。
冷冻设备是冷冻保存的一个关键挑战,然而在规模化生产中,审计追踪软件同样重要。该类软件是自体细胞疗法生态系统不可或缺的一部分,用于连接各个相关方(例如,单采中心、开发商、CDMO),并最大限度地减少因信息记录不完整或不准确而导致的产品交付延误的情况。TrakCel的OCELLOS等一站式解决方案能够集成管理COI和COC数据。例如,该平台能够记录从初始细胞采集到药品运输的所有数据,覆盖了临床和商业化的整个流程。
结论
如欲了解更多信息,请联系 apac.healthcare@lek.com。
L.E.K. Consulting是L.E.K. Consulting LLC的注册商标。本文档中提及的所有其他产品和品牌均为其各自所有者的财产。
© 2024 L.E.K. Consulting
尾注
1EvaluatePharma database
2L.E.K. analysis of Citeline’s Advanced Therapy Database
3L.E.K. analysis of PharmaProjects
4L.E.K. analysis of TrialTrove
5Piper Sandler, “Cell Therapy Compendium 5.0 – Tackling Solid Tumors.”
6Cytiva, “COGS process economics for autologous cell therapy.”
7L.E.K. research, analysis and interviews