美国国家综合癌症网络(NCCN)所提供的用药建议是公立和私营保险公司在决定新的和现有肿瘤药物报销覆盖范围时会考虑的黄金标准,对于适应症范围内的使用以及超适应症使用都是如此。在中国,肿瘤治疗市场正与国际接轨,临床指南以及医生的临床实践常常也以NCCN作为重要参考,NCCN的指导建议往往可以在药品正式获批前起到提前对临床医生进行教育的作用,为药品在中国上市后的临床使用奠定坚实的基础。
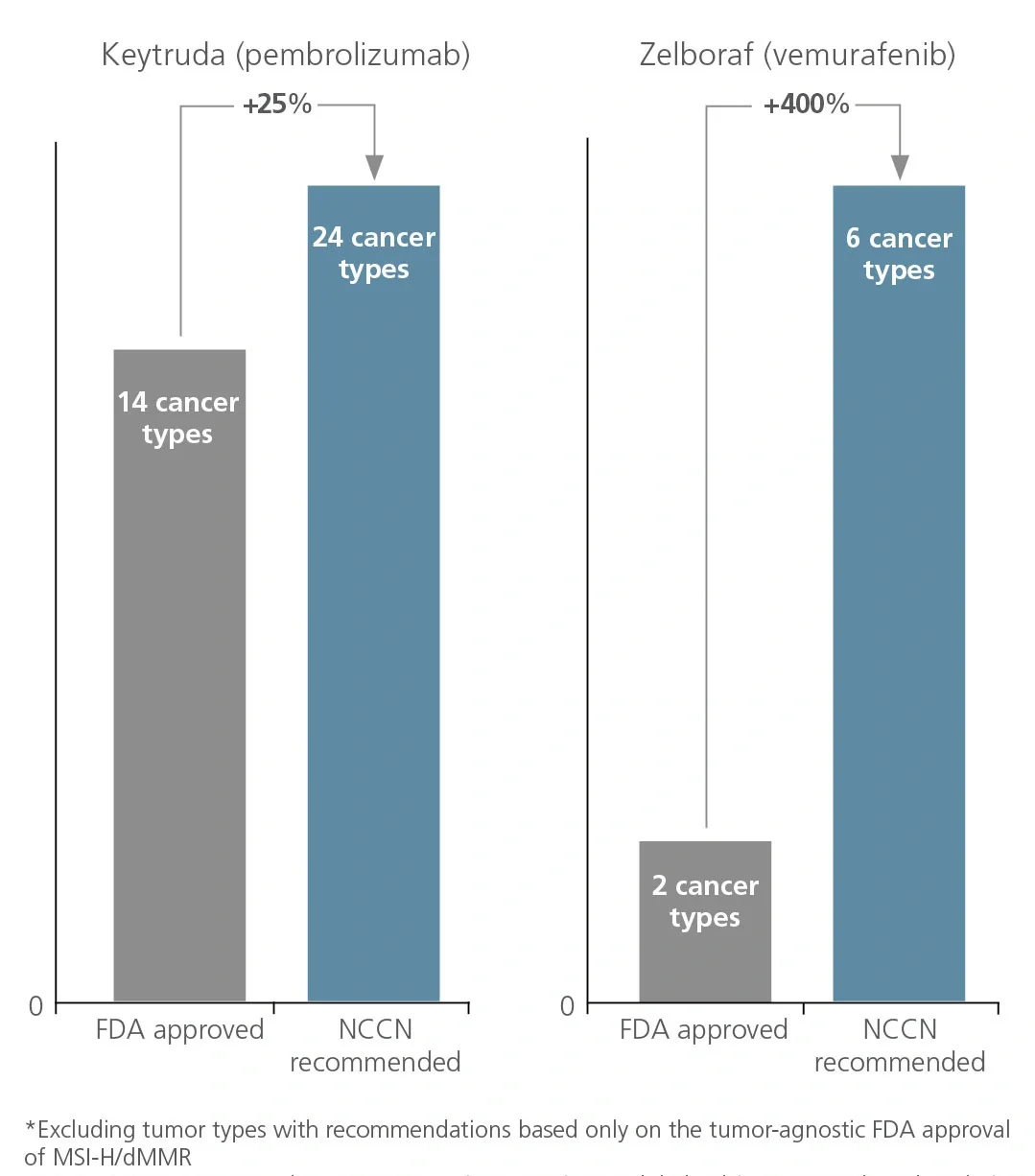
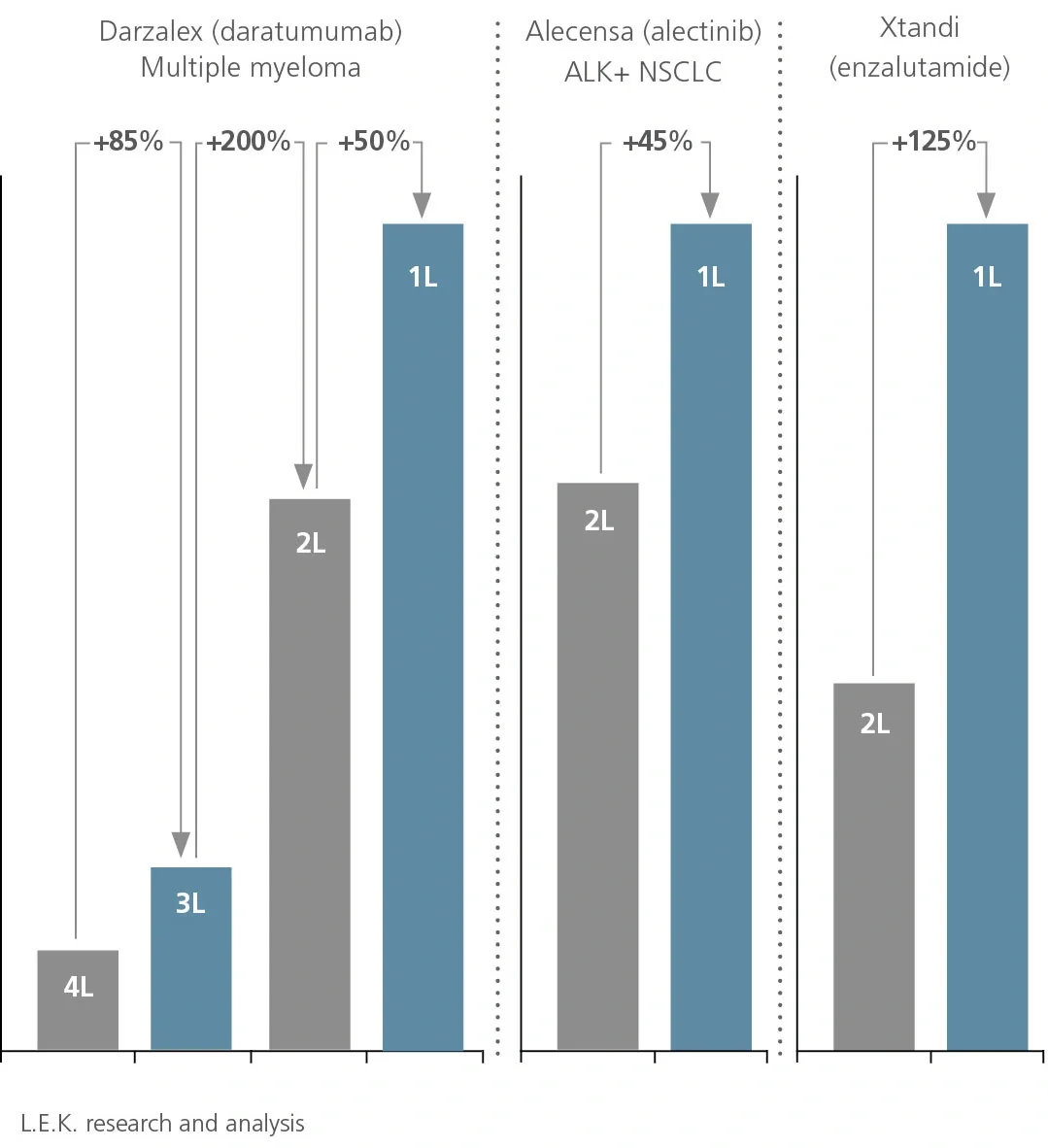
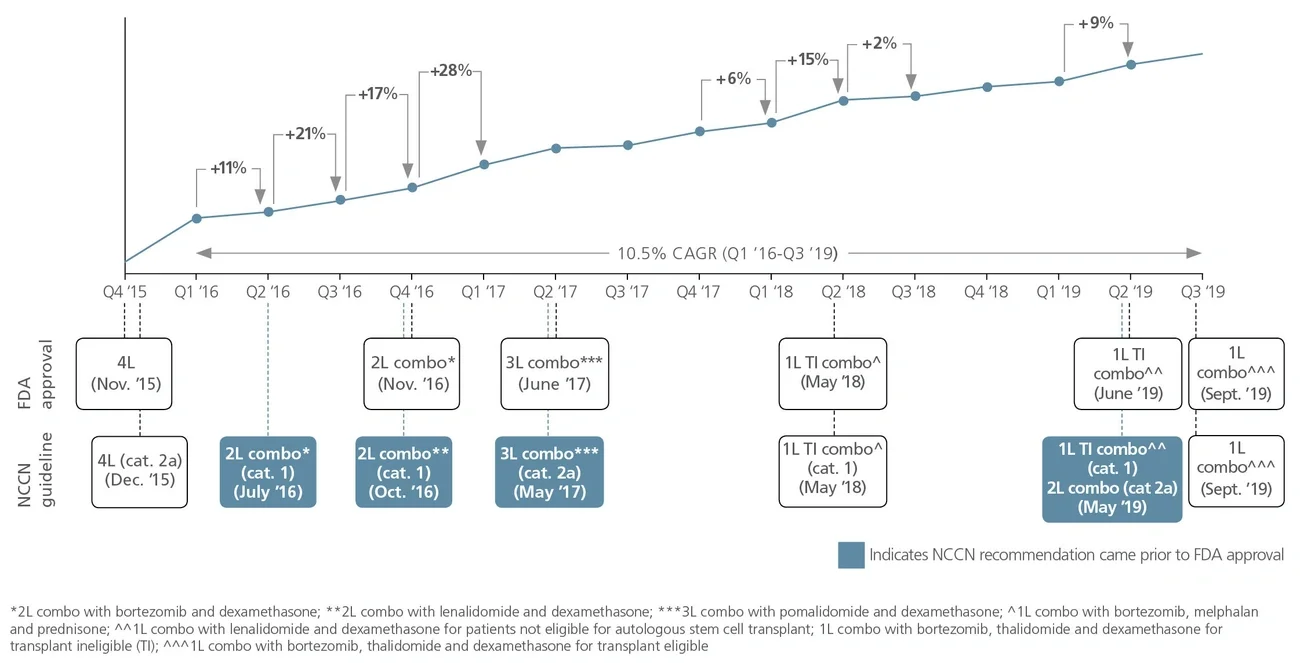
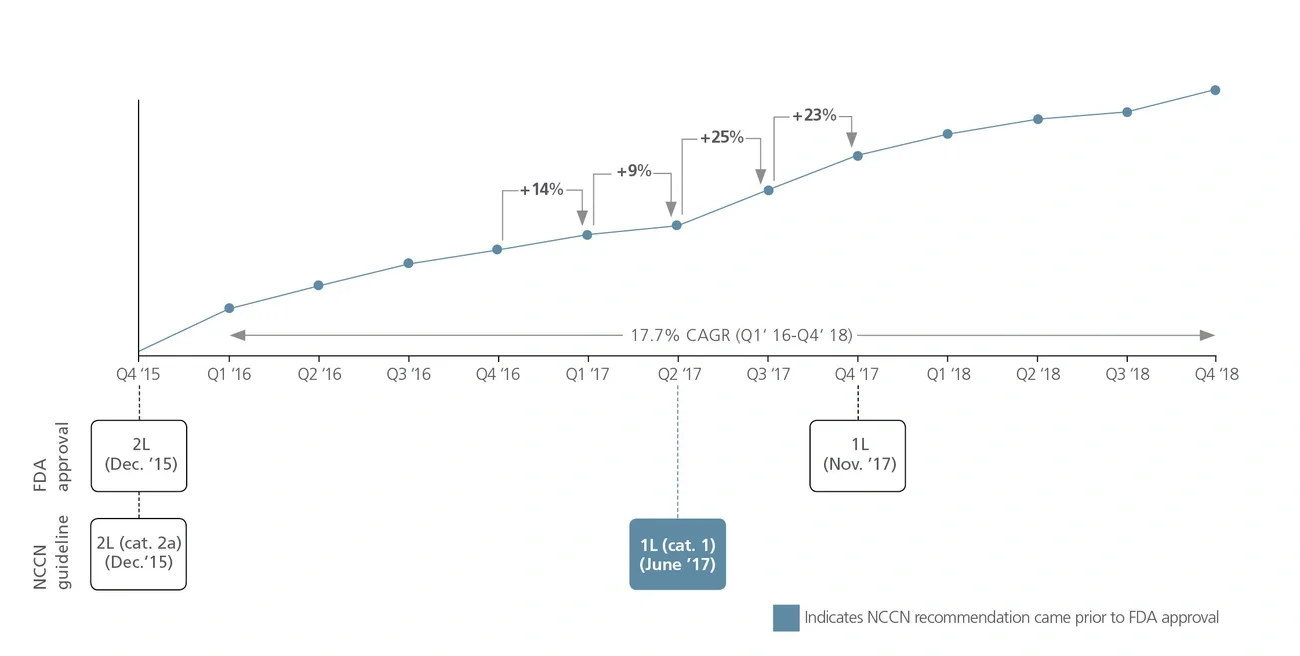
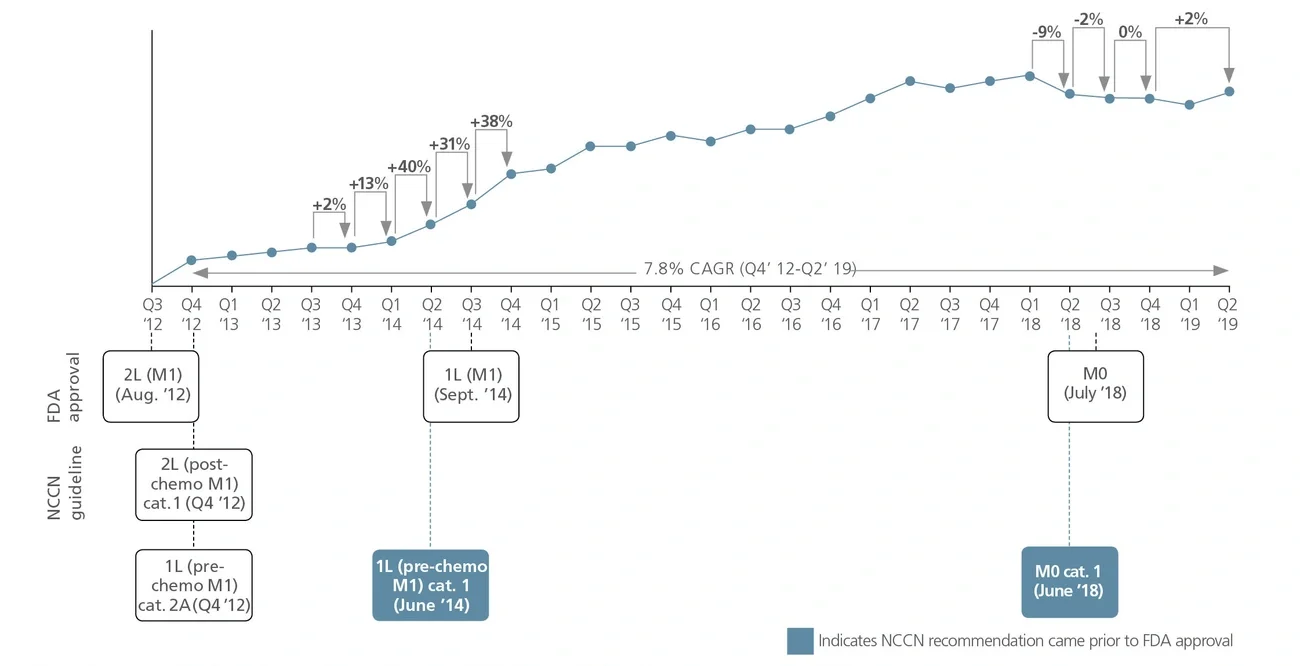
NCCN的建议用药推动了药物在更前线的治疗和其他适应症中的使用(即非主要/非注册适应症),包括超适应症使用。
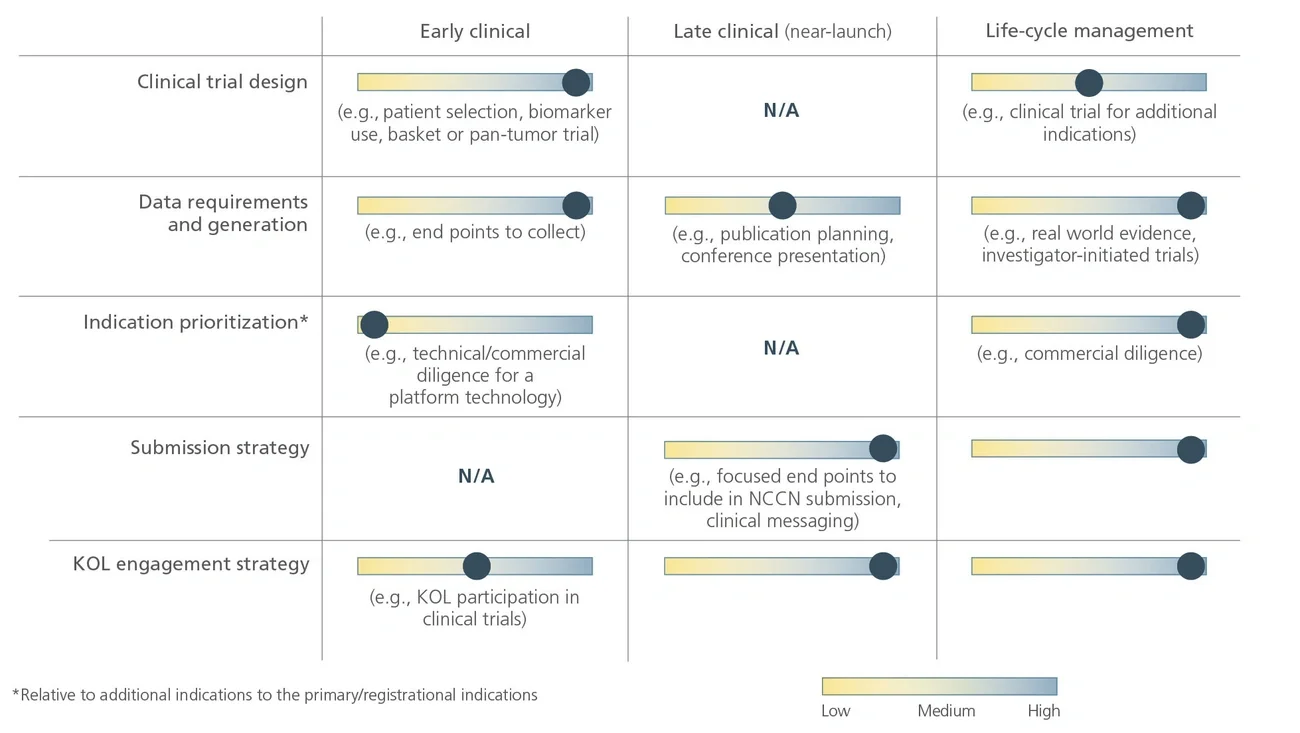
对于生物制药公司而言,制定一个有力的NCCN战略至关重要,该战略应该囊括药物生命周期所有阶段,并涉及到众多跨职能部门,从而最大限度地扩大肿瘤治疗的可及患者群体及其商业影响力。考虑到NCCN指南对中国医生在临床实践的影响力度,这一战略举措对生物制药公司在中国市场的拓展也发挥着十分重要的作用。
对于生物制药公司来说,肿瘤治疗是一个极具吸引力的市场。预计到2024年,全球总销售额将从2018年的约1250亿美元(约占全球市场份额的15%)增长到约2350亿美元(约占全球市场份额的20%),复合年增长率(CAGR)约为11%1 。此外,2011年至2016年期间推出的重磅药物中,约有35%-40%是肿瘤药物2 ,且大多数价格都很高。然而,尽管药物开发方面最近取得了长足进展,但几乎所有肿瘤类型中仍存在巨大的未满足需求,这吸引了大量的研发投资,已有数百家公司研发了数千种管线药物。这些复杂的市场动态为生物制药公司的战略规划带来了独特挑战,例如:
- 推动或赶上快速的创新步伐(例如:生物标志物为基础的泛肿瘤治疗的出现)以及不断发展的治疗模式,如靶向治疗3 和分期治疗
- 顺利通过充满不确定性、昂贵且漫长的FDA批准程序
- 在竞争日益激烈和以价值为中心的环境中获得有利的医保支付覆盖范围
- 使可及患者群体最大化
- 在药物生命周期的各个阶段都面临激烈的竞争
- 计划和管理适应症扩展,以延长治疗的生命周期
- 保障非FDA批准的适应症的报销(即“超适应症”或“扩展适应症”,这是许多肿瘤药物获得成功的重要组成部分
这些挑战也使得医生的医疗决策更加复杂(例如,医生需要思考如何选择治疗方案并确保能被报销),对病人、厂商、政府以及私人支付者而言都是如此。例如病人需要在不同竞争药品中做出选择;厂商需要思考如何提高新疗法的可及性;医保支付者则需要决定为药品提供怎样的报销水平。
美国医疗保险和医疗补助服务中心(CMS)认证药典的重要性
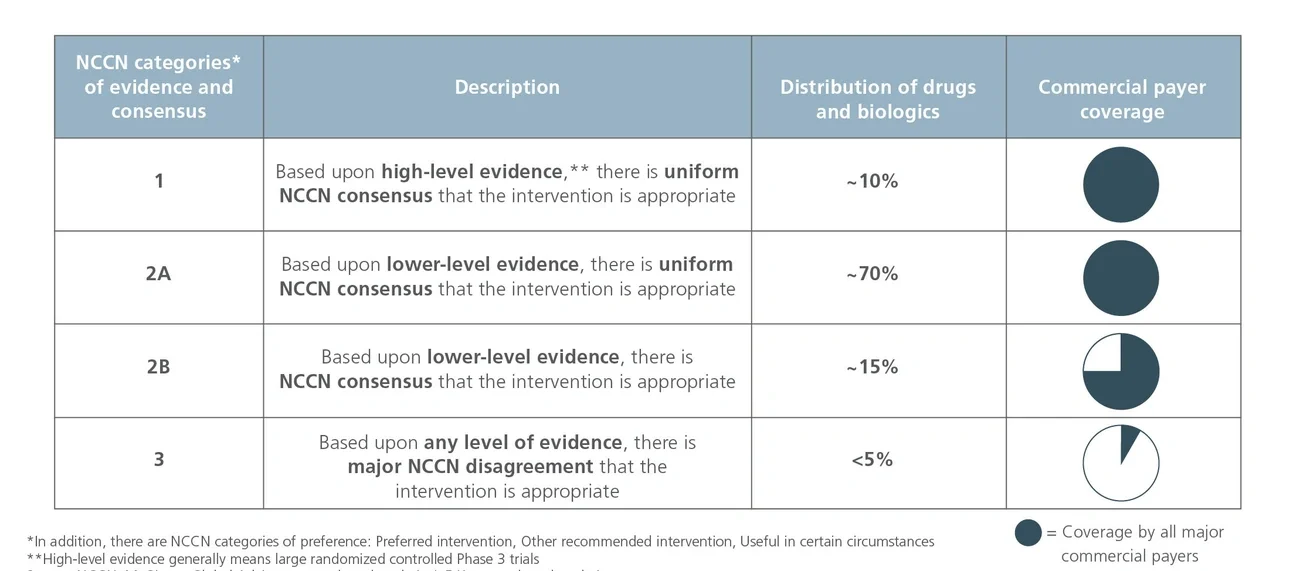
为了使上述群体的决策过程简单化,一些组织已经编撰药典,药典中包括了由专家根据药物特征相关的临床证据(例如:药理学特征、剂量、临床表现)汇编的信息,还可能包括药物的推荐用途。目前,已经有五种药典得到了美国联邦医疗保险和医疗补助服务中心(CMS)的认证,可用于确定药物从医学角度而言适用于哪些适应症,并为保险报销决策提供支撑信息(图1)。